- GIẢI BÀI TẬP HÓA 9 SÁCH GIÁO KHOA CHƯƠNG I – BÀI 1 : TÍNH CHẤT HÓA HỌC CỦA OXIT. KHÁI QUÁT VỀ SỰ PHÂN LOẠI OXIT
- GIẢI BÀI TẬP HÓA 9 CHƯƠNG I – BÀI 2 MỘT SỐ OXIT QUAN TRỌNG
- GIẢI BÀI TẬP HÓA 9 CHƯƠNG I – BÀI 3 TÍNH CHẤT HÓA HỌC CỦA AXIT
- GIẢI BÀI TẬP HÓA 9 SÁCH GIÁO KHOA CHƯƠNG I – BÀI 4 MỘT SỐ AXIT QUAN TRỌNG
- GIẢI BÀI TẬP HÓA 9 SÁCH GIÁO KHOA – CHƯƠNG I – BÀI 5 LUYỆN TẬP: TÍNH CHẤT CỦA OXIT VÀ AXIT
- GIẢI BÀI TẬP HÓA 9 SÁCH GIÁO KHOA – CHƯƠNG I – BÀI 6 THỰC HÀNH : TÍNH CHẤT HÓA HỌC CỦA OXIT VÀ AXIT
- GIẢI BÀI TẬP HÓA 9 SÁCH GIÁO KHOA – CHƯƠNG I – BÀI 8 MỘT SỐ BAZO QUAN TRỌNG
- GIẢI BÀI TẬP HÓA 9 SÁCH GIÁO KHOA – CHƯƠNG I – BÀI 7 TÍNH CHẤT HÓA HỌC CỦA BAZO
- GIẢI BÀI TẬP HÓA 9 SÁCH GIÁO KHOA – CHƯƠNG I – BÀI 9 TÍNH CHẤT HÓA HỌC CỦA MUỐI
- GIẢI BÀI TẬP HÓA 9 SÁCH GIÁO KHOA – CHƯƠNG I – BÀI 10 MỘT SỐ MUỐI QUAN TRỌNG
- GIẢI BÀI TẬP HÓA 9 SÁCH GIÁO KHOA – CHƯƠNG I – BÀI 12 MỐI QUAN HỆ GIỮA CÁC HỢP CHẤT VÔ CƠ
- GIẢI BÀI TẬP HÓA 9 SÁCH GIÁO KHOA – CHƯƠNG I – BÀI 11 PHÂN BÓN HÓA HỌC
- GIẢI BÀI TẬP HÓA 9 SÁCH GIÁO KHOA – CHƯƠNG I – BÀI 13 LUYỆN TẬP CHƯƠNG I CÁC HỢP CHẤT VÔ CƠ
- GIẢI BÀI TẬP HÓA 9 SÁCH GIÁO KHOA – CHƯƠNG II – BÀI 15 TÍNH CHẤT VẬT LÝ CỦA KIM LOẠI
- GIẢI BÀI TẬP HÓA 9 SÁCH GIÁO KHOA – CHƯƠNG II – BÀI 16 TÍNH CHẤT HÓA HỌC CỦA KIM LOẠI
- GIẢI BÀI TẬP HÓA 9 SÁCH GIÁO KHOA – CHƯƠNG I – BÀI 14 TÍNH CHẤT HÓA HỌC CỦA BAZO VA MUỐI
- GIẢI BÀI TẬP HÓA 9 SÁCH GIÁO KHOA – CHƯƠNG II – BÀI 17 DÃY HOẠT ĐỘNG HÓA HỌC CỦA KIM LOẠI
- GIẢI BÀI TẬP HÓA 9 SÁCH GIÁO KHOA – CHƯƠNG II – BÀI 18 NHÔM
- GIẢI BÀI TẬP HÓA 9 SÁCH GIÁO KHOA – CHƯƠNG II – BÀI 19 SẮT
- GIẢI BÀI TẬP HÓA 9 SÁCH GIÁO KHOA – CHƯƠNG II – BÀI 20 HỢP KIM SẮT : GANG THÉP
- GIẢI BÀI TẬP HÓA 9 SÁCH GIÁO KHOA – CHƯƠNG II – BÀI 21 SỰ ĂN MÒN KIM LOẠI VÀ BẢO VỆ KIM LOẠI KHÔNG BỊ ĂN MÒM
- GIẢI BÀI TẬP HÓA 9 SÁCH GIÁO KHOA – CHƯƠNG II – BÀI 22 LUYỆN TẬP CHƯƠNG II : KIM LOẠI
- GIẢI BÀI TẬP HÓA 9 SÁCH GIÁO KHOA – CHƯƠNG II – BÀI 23 THỰC HÀNH TÍNH CHẤT HÓA HỌC CỦA NHÔM VÀ SẮT
- GIẢI BÀI TẬP HÓA 9 SÁCH GIÁO KHOA – CHƯƠNG II – BÀI 24 ÔN TẬP HỌC KỲ 1
- GIẢI BÀI TẬP HÓA 9 SÁCH GIÁO KHOA – CHƯƠNG III – BÀI 25 TÍNH CHẤT CỦA PHI KIM
- GIẢI BÀI TẬP HÓA 9 SÁCH GIÁO KHOA – CHƯƠNG III – BÀI 26 CLO
- GIẢI BÀI TẬP HÓA 9 SÁCH GIÁO KHOA – CHƯƠNG III – BÀI 27 CACBON
- GIẢI BÀI TẬP HÓA 9 SÁCH GIÁO KHOA – CHƯƠNG III – BÀI 28 CÁC OXIT CỦA CÁCBON
- GIẢI BÀI TẬP HÓA 9 SÁCH GIÁO KHOA – CHƯƠNG III – BÀI 29 AXIT CACBONIC VÀ MUỐI CACBONAT
- GIẢI BÀI TẬP HÓA 9 SÁCH GIÁO KHOA – CHƯƠNG III – BÀI 30 SILIC. CÔNG NGHIỆP SILICAT
- GIẢI BÀI TẬP HÓA 9 SÁCH GIÁO KHOA – CHƯƠNG III – BÀI 31 SƠ LƯỢC VỀ BẢNG TUẦN HOÀN HÓA HỌC
- GIẢI BÀI TẬP HÓA 9 SÁCH GIÁO KHOA – CHƯƠNG III – BÀI 32 LUYỆN TẬP CHƯƠNG 3 PHI KIM. SƠ LƯỢC VỀ BẢNG TUẦN HOÀN HÓA HỌC
- GIẢI BÀI TẬP HÓA 9 SÁCH GIÁO KHOA – CHƯƠNG IV – BÀI 34 KHÁI NIỆM VỀ HỢP CHẤT HỮU CƠ VÀ HÓA HỌC HỮU CƠ
- GIẢI BÀI TẬP HÓA 9 SÁCH GIÁO KHOA – CHƯƠNG III – BÀI 33 THỰC HÀNH: TÍNH CHẤT HÓA HỌC CỦA PHI KIM VÀ HỢP CHẤT CỦA CHÚNG
- GIẢI BÀI TẬP HÓA 9 SÁCH GIÁO KHOA – CHƯƠNG IV – BÀI 36 METAN
- GIẢI BÀI TẬP HÓA 9 SÁCH GIÁO KHOA – CHƯƠNG IV – BÀI 35 CẤU TẠO PHÂN TỬ HỢP CHẤT HỮU CƠ
- GIẢI BÀI TẬP HÓA 9 SÁCH GIÁO KHOA – CHƯƠNG IV – BÀI 38 AXETILEN
- GIẢI BÀI TẬP HÓA 9 SÁCH GIÁO KHOA – CHƯƠNG IV – BÀI 39 BENZEN
- GIẢI BÀI TẬP HÓA 9 SÁCH GIÁO KHOA – CHƯƠNG IV – BÀI 37 ETILEN
- GIẢI BÀI TẬP HÓA 9 SÁCH GIÁO KHOA – CHƯƠNG IV – BÀI 41 NHIÊN LIỆU
- GIẢI BÀI TẬP HÓA 9 SÁCH GIÁO KHOA – CHƯƠNG IV – BÀI 42 LUYỆN TẬP CHƯƠNG 4; HIDROCACBON – NHIÊN LIỆU
- GIẢI BÀI TẬP HÓA 9 SÁCH GIÁO KHOA – CHƯƠNG IV – BÀI 43 THỰC HÀNH TÍNH CHẤT CỦA HIDROCACBON
- GIẢI BÀI TẬP HÓA 9 SÁCH GIÁO KHOA – CHƯƠNG V – BÀI 44 RƯỢU ETYLIC
- GIẢI BÀI TẬP HÓA 9 SÁCH GIÁO KHOA – CHƯƠNG V – BÀI 45 AXIT AXETIC
- GIẢI BÀI TẬP HÓA 9 SÁCH GIÁO KHOA – CHƯƠNG V – BÀI 46 MỐI LIÊN HỆ GIỮA ETILEN, RƯỢU ETYLIC VÀ AXIT AXETIC
- GIẢI BÀI TẬP HÓA 9 SÁCH GIÁO KHOA – CHƯƠNG V – BÀI 47 CHẤT BÉO
- GIẢI BÀI TẬP HÓA 9 SÁCH GIÁO KHOA – CHƯƠNG V – BÀI 48 LUYỆN TẬP: RƯỢU ETYLIC, AXIT AXETIC VÀ CHẤT BÉO
- GIẢI BÀI TẬP HÓA 9 SÁCH GIÁO KHOA – CHƯƠNG V – BÀI 49: THỰC HÀNH: TÍNH CHẤT CỦA RƯỢU VÀ AXIT
- GIẢI BÀI TẬP HÓA 9 SÁCH GIÁO KHOA – CHƯƠNG V – BÀI 50 GLUCOZO
- GIẢI BÀI TẬP HÓA 9 SÁCH GIÁO KHOA – CHƯƠNG V – BÀI 51 SACCAROZO
- GIẢI BÀI TẬP HÓA 9 SÁCH GIÁO KHOA – CHƯƠNG V – BÀI 52 TINH BỘT VÀ XENLULOZO
- GIẢI BÀI TẬP HÓA 9 SÁCH GIÁO KHOA – CHƯƠNG V – BÀI 53 PROTEIN
- GIẢI BÀI TẬP HÓA 9 SÁCH GIÁO KHOA – CHƯƠNG V – BÀI 54 POLIME
- GIẢI BÀI TẬP HÓA 9 SÁCH GIÁO KHOA – CHƯƠNG V – BÀI 55 THỰC HÀNH: TÍNH CHẤT CỦA GLUXIT
- GIẢI BÀI TẬP HÓA 9 SÁCH GIÁO KHOA – CHƯƠNG V – BÀI 56 ÔN TẬP CUỐI NĂM
Bài 24: Ôn tập học kì 1
Bài 1: Viết các phương trình hoa học biểu diễn các chuyển hóa sau đây :
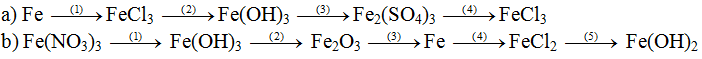
Lời giải:
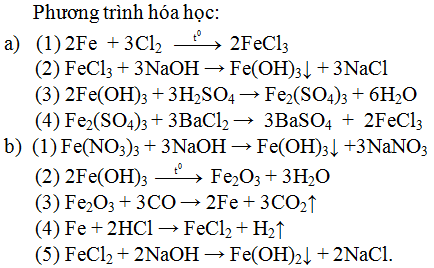
Bài 2: Cho bốn chất sau: Al, AlCl3, Al(OH)3, Al2O3. Hãy sắp xếp bốn chất này thành hai dãy chuyển hóa (mỗi dãy đều gòm 4 chất) và viết các phương trình hóa học tương ứng để thực hiện dãy chuyển hóa đó.
Lời giải:
Các dãy chuyển hóa có thể có:
Dãy biến hóa 1: Al → AlCl3 → Al(OH)3 → Al2O3
Dãy biến hóa 2: AlCl3 → Al(OH)3 → Al2O3 → Al
Bài 3: Có ba kim loại là nhôm, bạc, sắt. Hãy nêu phương pháp hóa học để nhận biết từng kim loại. Các dụng cụ hóa chất coi như có đủ. Viết các phương trình hóa học để nhận biết ba kim loại.
Lời giải:
Trích mẫu thử và đánh số thứ tự:
– Nhỏ dung dịch NaOH lần lượt vào 3 ống nghiệm chứa 3 kim loại trên
+ Kim loại nào tác dụng và có bọt khí bay lên là Al
+ 2 kim loại còn lại (Fe, Ag) không tác dụng.
PTHH: 2Al + 2NaOH + 2H2O → 2NaAlO2 + 3H2 ↑
– Cho dung dịch HCl vào hai kim loại Fe và Ag:
+ Kim loại nào tác dụng và có khí bay lên là Fe
+ Kim loại nào không tác dụng là Ag.
PTHH: Fe + 2HCl → FeCl2 + H2 ↑
Bài 4: Axit H2SO4 loãng phản ứng với tất cả các chất trong dãy chất nào dưới đây:
A. FeCl3, MgO, Cu, Ca(OH)2 .
B. NaOH, CuO, Ag, Zn.
C. Mg(OH)2, HgO, K2SO3, NaCl .
D. Al, Al2O3, Fe(OH)3, BaCl2.
Lời giải:
Axit H2SO4 loãng phản ứng được với dãy chất: Al, Al2O3, Fe(OH)2, BaCl2 hay D đúng.
Đáp án A loại Cu, FeCl3
Đáp án B loại Ag
Đáp án C loại NaCl
Bài 5: Dung dịch NaOH có phản ứng với tất cả các chất trong dãy nào sau đây:
A. FeCl3, MgCl2, CuO, HNO3.
B. H2SO4, SO2, CO2, FeCl2.
C. Al(OH)3, HCl, CuSO4, KNO3.
D. Al, HgO, H3PO4, BaCl2.
Lời giải:
Dung dịch NaOH phản ứng được với dãy chất: H2SO4, SO2, CO2, FeCl2 hay B đúng.
Đáp án A loại CuO
Đáp án C loại KNO3
Đáp án D loại MgO, BaCl2.
Bài 6: Sau khi làm thí nghiệm có những khí độc hại sau: HCl, H2S, CO2, SO2. Có thể dùng chất nào sau đây để loại bỏ chúng là tốt nhất?
A. Nước vôi trong.
B. Dung dịch HCl.
C. Dung dịch NaCl.
D. Nước.
Giải thích và viết phương trình phản ứng hóa học nếu có.
Lời giải:
Dùng phương án A, nước vôi trong là tốt nhất, vì nước vôi trong có phản ứng với tất cả các chất khí thải tạo thành chất kết tủa hay dung dịch.
Ca(OH)2 + 2HCl → CaCl2 + 2H2O.
H2S + Ca(OH)2 dư → CaS ↓ + 2H2O.
CO2 + Ca(OH)2 → CaCO3 ↓ + H2O.
SO2 + Ca(OH)2 → CaSO3 ↓ + H2O.
Bài 7: Bạc (dạng bột) có lẫn tạp chất đồng, nhôm. Dùng phương pháp hóa học để thu được bạc tinh khiết.
Lời giải:
Cho hỗn hợp vào dung dịch AgNO3 dư, đồng và nhôm sẽ phản ứng, kim loại thu được là Ag.
Cu + 2AgNO3 → Cu(NO3)2 + 2Ag ↓
Al + 3AgNO3 → Al(NO3)3 + 3Ag ↓
Bài 8: Trong phòng thí nghiệm, người ta làm khô các khí ẩm bằng cách dẫn khí này đi qua các bình có đựng các chất háo nước nhưng không có phản ứng với khí cần làm khô. Có các chất làm khô sau: H2SO4 đặc, CaO. Dùng hóa chất nào nói trên để làm khô mỗi khí ẩm sau đây: khí SO2, khí O2, khí CO2. Hãy giải thích sự lựa chọn đó.
Lời giải:
Có thể dùng H2SO4 đặc để làm khô các khí ẩm: SO2, CO2, O2 vì H2SO4 đặc có tính háo nước và không phản ứng với các khí này.
CaO khan có thể làm khô khí ẩm O2 vì không phản ứng với oxi nhưng CaO khan không dùng để làm khô khí ẩm SO2 và khí ẩm CO2 vì CaO khan tác dụng với khí ẩm SO2, CO2. Có thể xảy ra các phản ứng sau:
CaO + H2O → Ca(OH)2
CO2 + Ca(OH)2 → CaCO3 ↓ + H2O
SO2 + Ca(OH)2 → CaSO3 ↓ + H2O
Hoặc CaO + SO2 → CaSO3
CO2 + CaO → CaCO3
Bài 9: Cho 10g dung dịch muối sắt clorua 32,5% tác dụng với dung dịch bạc nitrat dư thì tạo thành 8,61g kết tủa. Hãy tìm công thức hóa học của muối sắt đã dùng.
Lời giải:
Gọi hóa trị của sắt trong muối là x.
mFeClx = 10 x 32,5 / 100 = 3,25g
Phương trình phản ứng hóa học:
FeClx + xAgNO3 → xAgCl ↓ + Fe(NO3)x
nAgCl = 8,61 / 143,5 = 0,06 mol.
nFeClx = 3,25 / (56 + 35,5x) mol.
Theo pt: nFeClx = 1/x . nAgCl
≥ 3,25 / (56 + 35,5x) = 0,6 / x.
Giải ra ta có x = 3. Vậy công thức hóa học của muối sắt clorua là FeCl3.
Bài 10: Cho 1,96g bột sắt vào 100ml dung dịch CuSO4 10% có khối lượng riêng là 1,12 g/ml.
a) Viết phương trình hóa học.
b) Xác định nồng độ mol của chất trong dung dịch khi phản ứng kết thúc. Giả thiết rằng thể tích của dung dịch sau phản ứng thay đổi không đáng kể.
Lời giải:
a) PTHH: Fe + CuSO4 → FeSO4 + Cu ↓
1 mol 1 mol 1 mol 1 mol
b) nFe = 1,96/56 = 0,035 (mol)
mdd CuSO4 = V.D = 1,12.100 = 112 (g)
mCuSO4 = (C% .mdd) / 100 = (112.10) / 100 = 11,2 (g)
nCuSO4 = 11,2 / 160 = 0,07 (mol)
Ta có tỉ lệ: 0,07/1 > 0,035/1 ⇒ CuSO4 dư
Theo pt nCuSO4 pư = nFeSO4 = 0,035 mol ⇒ nCuSO4 dư = 0,07 – 0,035 = 0,035 (mol)
Vdd = 100ml = 0,1 lít
CM CuSO4 dư = n / V = 0,035 / 0,1 = 0,35 (M)
CM FeSO4 = 0,035 / 0,1 = 0,35 (M)