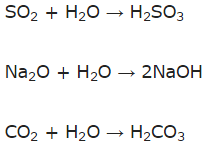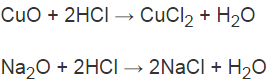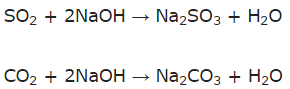- GIẢI BÀI TẬP HÓA 9 SÁCH GIÁO KHOA CHƯƠNG I – BÀI 1 : TÍNH CHẤT HÓA HỌC CỦA OXIT. KHÁI QUÁT VỀ SỰ PHÂN LOẠI OXIT
- GIẢI BÀI TẬP HÓA 9 CHƯƠNG I – BÀI 2 MỘT SỐ OXIT QUAN TRỌNG
- GIẢI BÀI TẬP HÓA 9 CHƯƠNG I – BÀI 3 TÍNH CHẤT HÓA HỌC CỦA AXIT
- GIẢI BÀI TẬP HÓA 9 SÁCH GIÁO KHOA CHƯƠNG I – BÀI 4 MỘT SỐ AXIT QUAN TRỌNG
- GIẢI BÀI TẬP HÓA 9 SÁCH GIÁO KHOA – CHƯƠNG I – BÀI 5 LUYỆN TẬP: TÍNH CHẤT CỦA OXIT VÀ AXIT
- GIẢI BÀI TẬP HÓA 9 SÁCH GIÁO KHOA – CHƯƠNG I – BÀI 6 THỰC HÀNH : TÍNH CHẤT HÓA HỌC CỦA OXIT VÀ AXIT
- GIẢI BÀI TẬP HÓA 9 SÁCH GIÁO KHOA – CHƯƠNG I – BÀI 8 MỘT SỐ BAZO QUAN TRỌNG
- GIẢI BÀI TẬP HÓA 9 SÁCH GIÁO KHOA – CHƯƠNG I – BÀI 7 TÍNH CHẤT HÓA HỌC CỦA BAZO
- GIẢI BÀI TẬP HÓA 9 SÁCH GIÁO KHOA – CHƯƠNG I – BÀI 9 TÍNH CHẤT HÓA HỌC CỦA MUỐI
- GIẢI BÀI TẬP HÓA 9 SÁCH GIÁO KHOA – CHƯƠNG I – BÀI 10 MỘT SỐ MUỐI QUAN TRỌNG
- GIẢI BÀI TẬP HÓA 9 SÁCH GIÁO KHOA – CHƯƠNG I – BÀI 12 MỐI QUAN HỆ GIỮA CÁC HỢP CHẤT VÔ CƠ
- GIẢI BÀI TẬP HÓA 9 SÁCH GIÁO KHOA – CHƯƠNG I – BÀI 11 PHÂN BÓN HÓA HỌC
- GIẢI BÀI TẬP HÓA 9 SÁCH GIÁO KHOA – CHƯƠNG I – BÀI 13 LUYỆN TẬP CHƯƠNG I CÁC HỢP CHẤT VÔ CƠ
- GIẢI BÀI TẬP HÓA 9 SÁCH GIÁO KHOA – CHƯƠNG II – BÀI 15 TÍNH CHẤT VẬT LÝ CỦA KIM LOẠI
- GIẢI BÀI TẬP HÓA 9 SÁCH GIÁO KHOA – CHƯƠNG II – BÀI 16 TÍNH CHẤT HÓA HỌC CỦA KIM LOẠI
- GIẢI BÀI TẬP HÓA 9 SÁCH GIÁO KHOA – CHƯƠNG I – BÀI 14 TÍNH CHẤT HÓA HỌC CỦA BAZO VA MUỐI
- GIẢI BÀI TẬP HÓA 9 SÁCH GIÁO KHOA – CHƯƠNG II – BÀI 17 DÃY HOẠT ĐỘNG HÓA HỌC CỦA KIM LOẠI
- GIẢI BÀI TẬP HÓA 9 SÁCH GIÁO KHOA – CHƯƠNG II – BÀI 18 NHÔM
- GIẢI BÀI TẬP HÓA 9 SÁCH GIÁO KHOA – CHƯƠNG II – BÀI 19 SẮT
- GIẢI BÀI TẬP HÓA 9 SÁCH GIÁO KHOA – CHƯƠNG II – BÀI 20 HỢP KIM SẮT : GANG THÉP
- GIẢI BÀI TẬP HÓA 9 SÁCH GIÁO KHOA – CHƯƠNG II – BÀI 21 SỰ ĂN MÒN KIM LOẠI VÀ BẢO VỆ KIM LOẠI KHÔNG BỊ ĂN MÒM
- GIẢI BÀI TẬP HÓA 9 SÁCH GIÁO KHOA – CHƯƠNG II – BÀI 22 LUYỆN TẬP CHƯƠNG II : KIM LOẠI
- GIẢI BÀI TẬP HÓA 9 SÁCH GIÁO KHOA – CHƯƠNG II – BÀI 23 THỰC HÀNH TÍNH CHẤT HÓA HỌC CỦA NHÔM VÀ SẮT
- GIẢI BÀI TẬP HÓA 9 SÁCH GIÁO KHOA – CHƯƠNG II – BÀI 24 ÔN TẬP HỌC KỲ 1
- GIẢI BÀI TẬP HÓA 9 SÁCH GIÁO KHOA – CHƯƠNG III – BÀI 25 TÍNH CHẤT CỦA PHI KIM
- GIẢI BÀI TẬP HÓA 9 SÁCH GIÁO KHOA – CHƯƠNG III – BÀI 26 CLO
- GIẢI BÀI TẬP HÓA 9 SÁCH GIÁO KHOA – CHƯƠNG III – BÀI 27 CACBON
- GIẢI BÀI TẬP HÓA 9 SÁCH GIÁO KHOA – CHƯƠNG III – BÀI 28 CÁC OXIT CỦA CÁCBON
- GIẢI BÀI TẬP HÓA 9 SÁCH GIÁO KHOA – CHƯƠNG III – BÀI 29 AXIT CACBONIC VÀ MUỐI CACBONAT
- GIẢI BÀI TẬP HÓA 9 SÁCH GIÁO KHOA – CHƯƠNG III – BÀI 30 SILIC. CÔNG NGHIỆP SILICAT
- GIẢI BÀI TẬP HÓA 9 SÁCH GIÁO KHOA – CHƯƠNG III – BÀI 31 SƠ LƯỢC VỀ BẢNG TUẦN HOÀN HÓA HỌC
- GIẢI BÀI TẬP HÓA 9 SÁCH GIÁO KHOA – CHƯƠNG III – BÀI 32 LUYỆN TẬP CHƯƠNG 3 PHI KIM. SƠ LƯỢC VỀ BẢNG TUẦN HOÀN HÓA HỌC
- GIẢI BÀI TẬP HÓA 9 SÁCH GIÁO KHOA – CHƯƠNG IV – BÀI 34 KHÁI NIỆM VỀ HỢP CHẤT HỮU CƠ VÀ HÓA HỌC HỮU CƠ
- GIẢI BÀI TẬP HÓA 9 SÁCH GIÁO KHOA – CHƯƠNG III – BÀI 33 THỰC HÀNH: TÍNH CHẤT HÓA HỌC CỦA PHI KIM VÀ HỢP CHẤT CỦA CHÚNG
- GIẢI BÀI TẬP HÓA 9 SÁCH GIÁO KHOA – CHƯƠNG IV – BÀI 36 METAN
- GIẢI BÀI TẬP HÓA 9 SÁCH GIÁO KHOA – CHƯƠNG IV – BÀI 35 CẤU TẠO PHÂN TỬ HỢP CHẤT HỮU CƠ
- GIẢI BÀI TẬP HÓA 9 SÁCH GIÁO KHOA – CHƯƠNG IV – BÀI 38 AXETILEN
- GIẢI BÀI TẬP HÓA 9 SÁCH GIÁO KHOA – CHƯƠNG IV – BÀI 39 BENZEN
- GIẢI BÀI TẬP HÓA 9 SÁCH GIÁO KHOA – CHƯƠNG IV – BÀI 37 ETILEN
- GIẢI BÀI TẬP HÓA 9 SÁCH GIÁO KHOA – CHƯƠNG IV – BÀI 41 NHIÊN LIỆU
- GIẢI BÀI TẬP HÓA 9 SÁCH GIÁO KHOA – CHƯƠNG IV – BÀI 42 LUYỆN TẬP CHƯƠNG 4; HIDROCACBON – NHIÊN LIỆU
- GIẢI BÀI TẬP HÓA 9 SÁCH GIÁO KHOA – CHƯƠNG IV – BÀI 43 THỰC HÀNH TÍNH CHẤT CỦA HIDROCACBON
- GIẢI BÀI TẬP HÓA 9 SÁCH GIÁO KHOA – CHƯƠNG V – BÀI 44 RƯỢU ETYLIC
- GIẢI BÀI TẬP HÓA 9 SÁCH GIÁO KHOA – CHƯƠNG V – BÀI 45 AXIT AXETIC
- GIẢI BÀI TẬP HÓA 9 SÁCH GIÁO KHOA – CHƯƠNG V – BÀI 46 MỐI LIÊN HỆ GIỮA ETILEN, RƯỢU ETYLIC VÀ AXIT AXETIC
- GIẢI BÀI TẬP HÓA 9 SÁCH GIÁO KHOA – CHƯƠNG V – BÀI 47 CHẤT BÉO
- GIẢI BÀI TẬP HÓA 9 SÁCH GIÁO KHOA – CHƯƠNG V – BÀI 48 LUYỆN TẬP: RƯỢU ETYLIC, AXIT AXETIC VÀ CHẤT BÉO
- GIẢI BÀI TẬP HÓA 9 SÁCH GIÁO KHOA – CHƯƠNG V – BÀI 49: THỰC HÀNH: TÍNH CHẤT CỦA RƯỢU VÀ AXIT
- GIẢI BÀI TẬP HÓA 9 SÁCH GIÁO KHOA – CHƯƠNG V – BÀI 50 GLUCOZO
- GIẢI BÀI TẬP HÓA 9 SÁCH GIÁO KHOA – CHƯƠNG V – BÀI 51 SACCAROZO
- GIẢI BÀI TẬP HÓA 9 SÁCH GIÁO KHOA – CHƯƠNG V – BÀI 52 TINH BỘT VÀ XENLULOZO
- GIẢI BÀI TẬP HÓA 9 SÁCH GIÁO KHOA – CHƯƠNG V – BÀI 53 PROTEIN
- GIẢI BÀI TẬP HÓA 9 SÁCH GIÁO KHOA – CHƯƠNG V – BÀI 54 POLIME
- GIẢI BÀI TẬP HÓA 9 SÁCH GIÁO KHOA – CHƯƠNG V – BÀI 55 THỰC HÀNH: TÍNH CHẤT CỦA GLUXIT
- GIẢI BÀI TẬP HÓA 9 SÁCH GIÁO KHOA – CHƯƠNG V – BÀI 56 ÔN TẬP CUỐI NĂM
Bài 5: Luyện tập: Tính chất hóa học của oxit và axit
Bài 1: Có những oxit sau: SO2, CuO, Na2O, CO2. Hãy cho biết những oxit nào tác dụng được với:
a) Nước.
b) Axit clohidric.
c) Natri hiđroxit?
Viết các phương trình hóa học.
Lời giải:
a) Những oxit tác dụng với nước: SO2, Na2O, CO2.
b) Những oxit tác dụng với dung dịch HCl: CuO, Na2O.
c) Những oxit tác dụng với dung dịch NaOH: CO2, SO2
Bài 2: Những oxit nào dưới đây có thể điều chế bằng:
a) Phản ứng hóa hợp? Viết phương trình hóa học.
b) Phản ứng hóa hợp và phản ứng phân hủy? Viết phương trình hóa học.
1) H2O.
2) CuO.
3) Na2O.
4) CO2.
5) P2O5.
Lời giải:
a) Cả 5 oxit đã cho có thể điều chế bằng phản ứng hóa hợp. Viết các phương trình hóa học
b) Các oxit có thể điều chế băng phản ứng hóa hợp và phản ứng phân hủy: CuO, CO2.
Cu(OH)2 to→ CuO + H2O
2Cu + O2 to→ 2CuO
CaCO3 to→ CaO + CO2
2Ca + O2 to→ 2CaO
Bài 3: Khí CO được dùng làm chất đốt trong công nghiệp, có lẫn tạp chất là các khí CO2 và SO2. Làm thế nào có thể loại bỏ những tạp chất ra khỏi CO bằng hóa chất rẻ tiền nhất? Viết các phương trình hóa học xảy ra.
Lời giải:
Cho hỗn hợp khí CO, CO2, SO2 lội từ từ qua dung dịch Ca(OH)2. CO2 và SO2 tác dụng với dung dịch Ca(OH)2 (dư) tạo chất không tan CaCO3 và CaSO3 còn lại khí CO không tác dụng thoát ra.
CO2 + Ca(OH)2 → CaCO3 ↓ + H2O
SO2 + Ca(OH)2 → CaSO3 ↓ + H2O.
Bài 4: Cần phải điều chế một lượng muối đồng sunfat. Phương pháp nào sau đây tiết kiệm được axit sunfuric:
a) Axit sunfuric tác dựng với đồng (II) oxit.
b) Axit sunfuric đặc tác dụng với kim loại đồng.
Giải thích cho câu trả lời.
Lời giải:
a) H2SO4 + CuO → CuSO4 + H2O (1)
b) Cu + 2H2SO4(đặc) → CuSO4 + SO2 ↑ + 2H2O (2)
Giả sử cần điều chế a mol CuSO4
Theo pt(1) nH2SO4 = nCuSO4 = a mol
Theo pt (2) nH2SO4 = 2.nCuSO4 = 2a mol
Do đó để tiết kiệm ta nên theo phản ứng (1) (phương pháp a) thì lượng axit H2SO4 sử dụng ít hơn ở phản ứng (2).
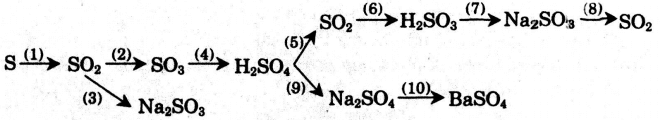
Bài 5: Hãy thực hiện những chuyển đổi hóa học sau bằng cách viết những phương trình phản ứng hóa học (ghi điều kiện của phản ứng, nếu có).
Lời giải:
Phương trình phản ứng:
1) S + O2 −to→ SO2
2) 2 SO2 + O2 −to, V2O5→ 2 SO3
3) SO2 + Na2 O → Na2SO3
4) SO3 + H2O → H2SO4
5) 2H2SO4 (đ) + Cu −to→ CuSO4 + SO2↑ + 2 H2O
6) SO2 + H2O -→ H2SO3
7) H2SO3 + 2 NaOH → Na2SO3 + 2H2O
8) Na2SO3 + 2HCl → 2 NaCl + SO2 ↑ + H2O
9) H2SO4 + 2 NaOH → Na2SO4 + 2H2O
10) Na2SO4 + BaCl2 → BaSO4 ↓ + 2 NaCl