- GIẢI BÀI TẬP HÓA 8 SÁCH GIÁO KHOA – CHƯƠNG I – BÀI 1 MỞ ĐẦU MÔN HÓA HỌC
- GIẢI BÀI TẬP HÓA 8 SÁCH GIÁO KHOA – CHƯƠNG I – BÀI 2 CHẤT
- GIẢI BÀI TẬP HÓA 8 SÁCH GIÁO KHOA – CHƯƠNG I – BÀI 3 BÀI THỰC HÀNH 1 – TÍNH CHẤT NÓNG CHẢY CỦA CHẤT – TÁCH CHẤT TỪ HỖN HỢP
- GIẢI BÀI TẬP HÓA 8 SÁCH GIÁO KHOA – CHƯƠNG I – BÀI 4 NGUYÊN TỬ
- GIẢI BÀI TẬP HÓA 8 SÁCH GIÁO KHOA – CHƯƠNG I – BÀI 5 NGUYÊN TỐ HÓA HỌC
- GIẢI BÀI TẬP HÓA 8 SÁCH GIÁO KHOA – CHƯƠNG I – BÀI 6 ĐƠN CHẤT VÀ HỢP CHẤT – PHÂN TỬ
- GIẢI BÀI TẬP HÓA 8 SÁCH GIÁO KHOA – CHƯƠNG I – BÀI 8 BÀI TẬP LUYỆN TẬP 1
- GIẢI BÀI TẬP HÓA 8 SÁCH GIÁO KHOA – CHƯƠNG I – BÀI 9 CÔNG THỨC HÓA TRỊ
- GIẢI BÀI TẬP HÓA 8 SÁCH GIÁO KHOA – CHƯƠNG I – BÀI 7 BÀI THỰC HÀNH 2
- GIẢI BÀI TẬP HÓA 8 SÁCH GIÁO KHOA – CHƯƠNG I – BÀI 10 HÓA TRỊ
- GIẢI BÀI TẬP HÓA 8 SÁCH GIÁO KHOA – CHƯƠNG I – BÀI 11 BÀI LUYỆN TẬP 2
- GIẢI BÀI TẬP HÓA 8 SÁCH GIÁO KHOA – CHƯƠNG II – BÀI 12 SỰ BIẾN ĐỔI CHẤT
- GIẢI BÀI TẬP HÓA 8 SÁCH GIÁO KHOA – CHƯƠNG II – BÀI 13 PHẢN ỨNG HÓA HỌC
- GIẢI BÀI TẬP HÓA 8 SÁCH GIÁO KHOA – CHƯƠNG II – BÀI 14 BÀI THỰC HÀNH 3
- GIẢI BÀI TẬP HÓA 8 SÁCH GIÁO KHOA – CHƯƠNG II – BÀI 15 ĐỊNH LUẬT BẢO TOÀN KHỐI LƯỢNG
- GIẢI BÀI TẬP HÓA 8 SÁCH GIÁO KHOA – CHƯƠNG II – BÀI 16 PHƯƠNG TRÌNH HÓA HỌC
- GIẢI BÀI TẬP HÓA 8 SÁCH GIÁO KHOA – CHƯƠNG II – BÀI 17 BÀI LUYỆN TẬP 3
- GIẢI BÀI TẬP HÓA 8 SÁCH GIÁO KHOA – CHƯƠNG III – BÀI 18 MOL
- GIẢI BÀI TẬP HÓA 8 SÁCH GIÁO KHOA – CHƯƠNG III – BÀI 19 CHUYỂN ĐỔI GIỮA KHỐI LƯỢNG THỂ TÍCH VÀ LƯỢNG CHẤT
- GIẢI BÀI TẬP HÓA 8 SÁCH GIÁO KHOA – CHƯƠNG III – BÀI 20 TỶ KHỐI CỦA CHẤT KHÍ
- GIẢI BÀI TẬP HÓA 8 SÁCH GIÁO KHOA – CHƯƠNG III – BÀI 21 TÍNH THEO CÔNG THỨC HÓA HỌC
- GIẢI BÀI TẬP HÓA 8 SÁCH GIÁO KHOA – CHƯƠNG III – BÀI 22 TÍNH THEO PHƯƠNG TRÌNH HÓA HỌC
- GIẢI BÀI TẬP HÓA 8 SÁCH GIÁO KHOA – CHƯƠNG III – BÀI 23 BÀI LUYỆN TẬP 4
- GIẢI BÀI TẬP HÓA 8 SÁCH GIÁO KHOA – CHƯƠNG IV – BÀI 25 SỰ OXI HÓA – PHẢN ỨNG HÓA HỢP – ỨNG DỤNG CỦA OXI
- GIẢI BÀI TẬP HÓA 8 SÁCH GIÁO KHOA – CHƯƠNG IV – BÀI 24 TÍNH CHẤT CỦA OXI
- GIẢI BÀI TẬP HÓA 8 SÁCH GIÁO KHOA – CHƯƠNG IV – BÀI 26 OXIT
- GIẢI BÀI TẬP HÓA 8 SÁCH GIÁO KHOA – CHƯƠNG IV – BÀI 27 ĐIỀU CHẾ OXI – PHẢN ỨNG PHÂN HỦY
- GIẢI BÀI TẬP HÓA 8 SÁCH GIÁO KHOA – CHƯƠNG IV – BÀI 29 BÀI LUYỆN TẬP 5
- GIẢI BÀI TẬP HÓA 8 SÁCH GIÁO KHOA – CHƯƠNG IV – BÀI 30 BÀI THỰC HÀNH 4
- GIẢI BÀI TẬP HÓA 8 SÁCH GIÁO KHOA – CHƯƠNG IV – BÀI 28 KHÔNG KHÍ – SỰ CHÁY
- GIẢI BÀI TẬP HÓA 8 SÁCH GIÁO KHOA – CHƯƠNG V – BÀI 31 TÍNH CHẤT – ỨNG DỤNG CỦA HIDRO
- GIẢI BÀI TẬP HÓA 8 SÁCH GIÁO KHOA – CHƯƠNG V – BÀI 32 PHẢN ỨNG OXI HÓA KHỬ
- GIẢI BÀI TẬP HÓA 8 SÁCH GIÁO KHOA – CHƯƠNG V – BÀI 33 ĐIỀU CHẾ KHÍ HIDDRO – PHẢN ỨNG THẾ
- GIẢI BÀI TẬP HÓA 8 SÁCH GIÁO KHOA – CHƯƠNG V – BÀI 34 BÀI LUYỆN TẬP 6
- GIẢI BÀI TẬP HÓA 8 SÁCH GIÁO KHOA – CHƯƠNG V – BÀI 35 BÀI THỰC HÀNH 5
- GIẢI BÀI TẬP HÓA 8 SÁCH GIÁO KHOA – CHƯƠNG V – BÀI 36 NƯỚC
- GIẢI BÀI TẬP HÓA 8 SÁCH GIÁO KHOA – CHƯƠNG V – BÀI 37 AXIT – BAZO – MUỐI
- GIẢI BÀI TẬP HÓA 8 SÁCH GIÁO KHOA – CHƯƠNG V – BÀI 38 BÀI LUYỆN TẬP 7
- GIẢI BÀI TẬP HÓA 8 SÁCH GIÁO KHOA – CHƯƠNG V – BÀI 39 BÀI THỰC HÀNH 6
- GIẢI BÀI TẬP HÓA 8 SÁCH GIÁO KHOA – CHƯƠNG VI – BÀI 40 DUNG DỊCH
- GIẢI BÀI TẬP HÓA 8 SÁCH GIÁO KHOA – CHƯƠNG VI – BÀI 41 ĐỘ TAN CỦA MỘT CHẤT TRONG NƯỚC
- GIẢI BÀI TẬP HÓA 8 SÁCH GIÁO KHOA – CHƯƠNG VI – BÀI 42 NỒNG ĐỘ DUNG DỊCH
- GIẢI BÀI TẬP HÓA 8 SÁCH GIÁO KHOA – CHƯƠNG VI – BÀI 43 PHA CHẾ DUNG DỊCH
- GIẢI BÀI TẬP HÓA 8 SÁCH GIÁO KHOA – CHƯƠNG VI – BÀI 44 BÀI LUYỆN TẬP 8
- GIẢI BÀI TẬP HÓA 8 SÁCH GIÁO KHOA – CHƯƠNG VI – BÀI 45 BÀI THỰC HÀNH 7
Bài 27: Điều chế khí oxi – Phản ứng phân hủy
Bài 1: Những chất nào trong số các chất sau được dùng để điều chế oxi trong phòng thí nghiệm?
a) Fe3O4.
b) KClO3.
c) KMnO4.
d) CaCO3.
e) Không khí.
g) H2O.
Lời giải:
Chọn đáp án: b) KClO3. c) KMnO4.
2KClO3 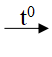
2KMnO4 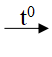
Bài 2: Sự khác nhau về cách điều chế oxi trong phòng thí nghiệm và trong công nghiệp về nguyên liệu, sản lượng và giá thành?
Lời giải:
Sự khác nhau về cách điều chế oxi trong phòng thí nghiệm (PTN) và trong công nghiệp (CN).
– Nguyên liệu:
PTN: KClO3 hoặc KMnO4(chất giàu oxi, phản ứng thực hiện nhanh, dễ dàng)
CN: Không khí và nước.
– Sản lượng:
PTN: Thể tích nhỏ dùng cho thí nghiệm.
CN: Sản lượng lớn dùng cho công nghiệp và y tế.
– Giá thành:
PTN: Giá thành cao.
CN: Giá thành hạ vì nguyên liệu là không khí và nước.
Cách điều chế trong CN và PTN cũng khác nhau, trong PTN nhiệt phân KClO3 (hoặc KMnO4) còn trong CN từ hóa lỏng không khí hay điện phân nước.
Bài 3: Sự khác nhau giữa phản ứng phân hủy và phản ứng hóa hợp? Dẫn ra 2 thí dụ để minh họa.
Lời giải:
Sự khác nhau giữa phản ứng phân hủy và phản ứng hóa hợp.
Phản ứng hóa hợp là phản ứng hóa học trong đó chỉ có một chất mới được tạo thành từ hai hay nhiều chất ban đầu.
Thí dụ:
CaO + CO2 → CaCO3.
2Cu + O2 → 2CuO.
Phản ứng phân hủy là phản ứng hóa học trong đó một chất sinh ra hai hay nhiều chất mới.
Thí dụ:
2HgO → 2Hg + O2↑
2KClO3 → 2KCl + 3O2
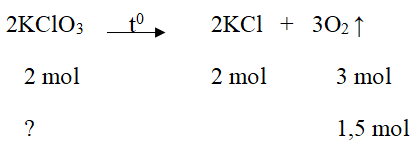
Bài 4: Tính số mol và số gam kali clorat cần thiết để điều chế được:
a) 48g khí oxi.
b) 44,8 lít khí oxi (ở đktc).
Lời giải:
a) PTPỨ:
nO2 = 48/32 = 1,5 (mol); nKClO3 = (2/3). 1,5 = 1 (mol)
mKClO3 = n.M = 1.122,5 = 122,5 (g)
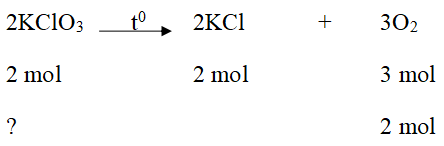
b) PTPỨ:
nO2 = 44,8/22,4 = 2 mol
nKClO3 = (2/3). 2 = 4/3 (mol)
mKClO3 = n.M = (4/3).122,5 = 163,3 (g)
Bài 4: Tính số mol và số gam kali clorat cần thiết để điều chế được:
a) 48g khí oxi.
b) 44,8 lít khí oxi (ở đktc).
Lời giải:
a) PTPỨ:
nO2 = 48/32 = 1,5 (mol); nKClO3 = (2/3). 1,5 = 1 (mol)
mKClO3 = n.M = 1.122,5 = 122,5 (g)
b) PTPỨ:
nO2 = 44,8/22,4 = 2 mol
nKClO3 = (2/3). 2 = 4/3 (mol)
mKClO3 = n.M = (4/3).122,5 = 163,3 (g)
Bài 6: Trong phòng thí nghiệm người ta điều chế oxit sắt từ Fe3O4 bằng cách dùng oxi hóa sắt ở nhiệt độ cao.
a) Tính số gam sắt và oxi cần dùng để điều chế được 2,32g oxi sắt từ?
b) Tính số gam kali pemanganat KMnO4 cần dùng để có được lượng oxi dùng cho phản ứng trên, biết rằng khi nung nóng 2 mol KMnO4 thì thu được 1 mol O2.
Lời giải:
a) Phương trình hóa học của phản ứng:
3Fe + 2O2 → Fe3O4.
nFe3O4 = 2,32/232 = 0,01 mol.
nFe= 0,01 .3 = 0,03 mol.
nO2= 0,01 .2 = 0,02 mol.
mFe = 0,03.56 = 1,68g.
mO2 = 0,02.32 = 0,64g.
b) Phương trình phản ứng nhiệt phân KMnO4:
2KMnO4 → K2MnO4 + MnO2 + O2
nKMnO4 = 0,02.2 = 0,04 mol.
mKMnO4 = 0,04 .158 = 6,32g.