- GIẢI BÀI TẬP HÓA 8 SÁCH GIÁO KHOA – CHƯƠNG I – BÀI 1 MỞ ĐẦU MÔN HÓA HỌC
- GIẢI BÀI TẬP HÓA 8 SÁCH GIÁO KHOA – CHƯƠNG I – BÀI 2 CHẤT
- GIẢI BÀI TẬP HÓA 8 SÁCH GIÁO KHOA – CHƯƠNG I – BÀI 3 BÀI THỰC HÀNH 1 – TÍNH CHẤT NÓNG CHẢY CỦA CHẤT – TÁCH CHẤT TỪ HỖN HỢP
- GIẢI BÀI TẬP HÓA 8 SÁCH GIÁO KHOA – CHƯƠNG I – BÀI 4 NGUYÊN TỬ
- GIẢI BÀI TẬP HÓA 8 SÁCH GIÁO KHOA – CHƯƠNG I – BÀI 5 NGUYÊN TỐ HÓA HỌC
- GIẢI BÀI TẬP HÓA 8 SÁCH GIÁO KHOA – CHƯƠNG I – BÀI 6 ĐƠN CHẤT VÀ HỢP CHẤT – PHÂN TỬ
- GIẢI BÀI TẬP HÓA 8 SÁCH GIÁO KHOA – CHƯƠNG I – BÀI 8 BÀI TẬP LUYỆN TẬP 1
- GIẢI BÀI TẬP HÓA 8 SÁCH GIÁO KHOA – CHƯƠNG I – BÀI 9 CÔNG THỨC HÓA TRỊ
- GIẢI BÀI TẬP HÓA 8 SÁCH GIÁO KHOA – CHƯƠNG I – BÀI 7 BÀI THỰC HÀNH 2
- GIẢI BÀI TẬP HÓA 8 SÁCH GIÁO KHOA – CHƯƠNG I – BÀI 10 HÓA TRỊ
- GIẢI BÀI TẬP HÓA 8 SÁCH GIÁO KHOA – CHƯƠNG I – BÀI 11 BÀI LUYỆN TẬP 2
- GIẢI BÀI TẬP HÓA 8 SÁCH GIÁO KHOA – CHƯƠNG II – BÀI 12 SỰ BIẾN ĐỔI CHẤT
- GIẢI BÀI TẬP HÓA 8 SÁCH GIÁO KHOA – CHƯƠNG II – BÀI 13 PHẢN ỨNG HÓA HỌC
- GIẢI BÀI TẬP HÓA 8 SÁCH GIÁO KHOA – CHƯƠNG II – BÀI 14 BÀI THỰC HÀNH 3
- GIẢI BÀI TẬP HÓA 8 SÁCH GIÁO KHOA – CHƯƠNG II – BÀI 15 ĐỊNH LUẬT BẢO TOÀN KHỐI LƯỢNG
- GIẢI BÀI TẬP HÓA 8 SÁCH GIÁO KHOA – CHƯƠNG II – BÀI 16 PHƯƠNG TRÌNH HÓA HỌC
- GIẢI BÀI TẬP HÓA 8 SÁCH GIÁO KHOA – CHƯƠNG II – BÀI 17 BÀI LUYỆN TẬP 3
- GIẢI BÀI TẬP HÓA 8 SÁCH GIÁO KHOA – CHƯƠNG III – BÀI 18 MOL
- GIẢI BÀI TẬP HÓA 8 SÁCH GIÁO KHOA – CHƯƠNG III – BÀI 19 CHUYỂN ĐỔI GIỮA KHỐI LƯỢNG THỂ TÍCH VÀ LƯỢNG CHẤT
- GIẢI BÀI TẬP HÓA 8 SÁCH GIÁO KHOA – CHƯƠNG III – BÀI 20 TỶ KHỐI CỦA CHẤT KHÍ
- GIẢI BÀI TẬP HÓA 8 SÁCH GIÁO KHOA – CHƯƠNG III – BÀI 21 TÍNH THEO CÔNG THỨC HÓA HỌC
- GIẢI BÀI TẬP HÓA 8 SÁCH GIÁO KHOA – CHƯƠNG III – BÀI 22 TÍNH THEO PHƯƠNG TRÌNH HÓA HỌC
- GIẢI BÀI TẬP HÓA 8 SÁCH GIÁO KHOA – CHƯƠNG III – BÀI 23 BÀI LUYỆN TẬP 4
- GIẢI BÀI TẬP HÓA 8 SÁCH GIÁO KHOA – CHƯƠNG IV – BÀI 25 SỰ OXI HÓA – PHẢN ỨNG HÓA HỢP – ỨNG DỤNG CỦA OXI
- GIẢI BÀI TẬP HÓA 8 SÁCH GIÁO KHOA – CHƯƠNG IV – BÀI 24 TÍNH CHẤT CỦA OXI
- GIẢI BÀI TẬP HÓA 8 SÁCH GIÁO KHOA – CHƯƠNG IV – BÀI 26 OXIT
- GIẢI BÀI TẬP HÓA 8 SÁCH GIÁO KHOA – CHƯƠNG IV – BÀI 27 ĐIỀU CHẾ OXI – PHẢN ỨNG PHÂN HỦY
- GIẢI BÀI TẬP HÓA 8 SÁCH GIÁO KHOA – CHƯƠNG IV – BÀI 29 BÀI LUYỆN TẬP 5
- GIẢI BÀI TẬP HÓA 8 SÁCH GIÁO KHOA – CHƯƠNG IV – BÀI 30 BÀI THỰC HÀNH 4
- GIẢI BÀI TẬP HÓA 8 SÁCH GIÁO KHOA – CHƯƠNG IV – BÀI 28 KHÔNG KHÍ – SỰ CHÁY
- GIẢI BÀI TẬP HÓA 8 SÁCH GIÁO KHOA – CHƯƠNG V – BÀI 31 TÍNH CHẤT – ỨNG DỤNG CỦA HIDRO
- GIẢI BÀI TẬP HÓA 8 SÁCH GIÁO KHOA – CHƯƠNG V – BÀI 32 PHẢN ỨNG OXI HÓA KHỬ
- GIẢI BÀI TẬP HÓA 8 SÁCH GIÁO KHOA – CHƯƠNG V – BÀI 33 ĐIỀU CHẾ KHÍ HIDDRO – PHẢN ỨNG THẾ
- GIẢI BÀI TẬP HÓA 8 SÁCH GIÁO KHOA – CHƯƠNG V – BÀI 34 BÀI LUYỆN TẬP 6
- GIẢI BÀI TẬP HÓA 8 SÁCH GIÁO KHOA – CHƯƠNG V – BÀI 35 BÀI THỰC HÀNH 5
- GIẢI BÀI TẬP HÓA 8 SÁCH GIÁO KHOA – CHƯƠNG V – BÀI 36 NƯỚC
- GIẢI BÀI TẬP HÓA 8 SÁCH GIÁO KHOA – CHƯƠNG V – BÀI 37 AXIT – BAZO – MUỐI
- GIẢI BÀI TẬP HÓA 8 SÁCH GIÁO KHOA – CHƯƠNG V – BÀI 38 BÀI LUYỆN TẬP 7
- GIẢI BÀI TẬP HÓA 8 SÁCH GIÁO KHOA – CHƯƠNG V – BÀI 39 BÀI THỰC HÀNH 6
- GIẢI BÀI TẬP HÓA 8 SÁCH GIÁO KHOA – CHƯƠNG VI – BÀI 40 DUNG DỊCH
- GIẢI BÀI TẬP HÓA 8 SÁCH GIÁO KHOA – CHƯƠNG VI – BÀI 41 ĐỘ TAN CỦA MỘT CHẤT TRONG NƯỚC
- GIẢI BÀI TẬP HÓA 8 SÁCH GIÁO KHOA – CHƯƠNG VI – BÀI 42 NỒNG ĐỘ DUNG DỊCH
- GIẢI BÀI TẬP HÓA 8 SÁCH GIÁO KHOA – CHƯƠNG VI – BÀI 43 PHA CHẾ DUNG DỊCH
- GIẢI BÀI TẬP HÓA 8 SÁCH GIÁO KHOA – CHƯƠNG VI – BÀI 44 BÀI LUYỆN TẬP 8
- GIẢI BÀI TẬP HÓA 8 SÁCH GIÁO KHOA – CHƯƠNG VI – BÀI 45 BÀI THỰC HÀNH 7
Bài 19: Chuyển đổi giữa khối lượng thể tích và lượng chất
Bài 1: Kết luận nào đúng?
Nếu hai chất khí khác nhau mà có thể tích bằng nhau (đo cùng nhiệt độ và áp suất) thì:
a) Chúng có cùng số mol chất.
b) Chúng có cùng khối lượng.
c) Chúng có cùng số phân tử.
d) Không có kết luận được điều gì cả.
Lời giải:
Chọn đáp án đúng: a) và c)
Vì V = n. 22,4 nên 2 chất khí có cùng V sẽ có cùng số mol chất ⇒ a đúng
1 mol chứa 6.1023 nguyên tử hoặc phân tử nên cùng số mol sẽ có cùng số phân tử ⇒ c đúng
Khối lượng m = M.n phụ thuộc vào phân tử khối và nguyên tử khối ⇒ b sai
Bài 2: Câu nào diễn tả đúng?
Thể tích mol của chất khí phụ thuộc vào:
a) Nhiệt độ của chất khí.
b) Khối lượng mol của chất khí.
c) Bản chất của chất khí.
d) Áp suất của chất khí.
Lời giải:
Chọn đáp án: a) và d).
Ở điều kiện tiêu chuẩn (0°, 1atm) 1 mol khí có thể tích là 22,4l
Ở đk thường (20°, 1atm) 1 mol khí có thể tích là 24l
⇒ V phụ thuộc vào nhiệt độ và áp suất ⇒ a, d đúng
Với mọi chất khí ở đktc ta có V = n.22,4 ⇒ V không phụ thuộc vào khối lượng mol của chất khí và bản chất của chất khí ⇒ b,c sai.
Bài 3: Hãy tính:
a) Số mol của : 28g Fe 64g Cu 5,4g Al.
b) Thể tích khí (đktc) của 0,175 mol CO2; 1,25 mol H2; 3 mol N2.
c) Số mol và thể tích của hỗn hợp khí (dktc) gồm có 0,44g CO2 0,04g H2 và 0,56g N2.
Lời giải:
a) nFe = 28/56 = 0,5 mol; nCu = 64/64 = 1 mol; nAl = 5.4/27= 0,2 mol.
b) VCO2 = 22,4 .0,175 = 3,92l.
VH2 = 22,4 .1,25 = 28l.
VN2 = 22,4.3 = 67,2l.
c) Số mol của hỗn hợp khí bằng tổng số mol của từng khí.
nCO2 = 0,44/44 = 0,01 mol.
nH2 = 0,04/2 = 0,02 mol.
nN2 = 0,56/22,4 = 0,02 mol.
nhh = nCO2 + nH2 + nN2 = 0,01 + 0,02 + 0,02 = 0,05 mol
Vhh khí = (0,01 + 0,02 + 0,02) . 22,4 = 1,12l.
Bài 4: Hãy cho biết khối lượng của những lượng chất sau:
a) 0,5 mol nguyên tử N; 0,01 mol nguyên tử Cl; 3 mol nguyên tử O;
b) 0,5 mol phân tử N2; 0,10 mol phân tử Cl2 ; 3 mol phân tử O2
c) 0,1 mol Fe ; 2,15 mol Cu, 0,8 mol H2SO4 ; 0,5 mol CuSO4
Lời giải:
a) mN = 0,5 .14 = 7g.
mCl = 0,1 .35.5 = 3.55g
mO = 3.16 = 48g.
b) mN2 = 0,5 .28 = 14g.
mCl2 = 0,1 .71 = 7,1g
mO2 = 3.32 =96g
c) mFe = 0,1 .56 =5,6g mCu = 2,15.64 = 137,6g
mH2SO4 = 0,8.98 = 78,4g.
mCuSO4 = 0,5 .160 = 80g
Bài 5: Có 100g khí oxi và 100g khí cacbon đioxit cả hai khí đều ở 25oC và 1atm. Biết rằng thể tích mol khí ở những điều kiện này có thể tích là 24l. Nếu trộn hai khối lượng khí trên với nhau (không có phản ứng xảy ra) thì hỗn hợp khí thu được có thể tích là bao nhiêu?
Lời giải:
nO2 = 100/32 = 3,125 mol;
nCO2 = 100/44 = 2,273 mol;
Thể tích của hỗn hợp khí ở 20°C và 1atm
Vhh = 24.(nO2 + nCO2) = 24.(3,125 + 2,273) = 129,552 l.
Bài 6: Hãy vẽ những hình khối chữ nhật để so sánh thể tích các khí sau (đktc): 1gH2 ; 8g O2 ; 3,5gN2 ; 33gCO2
Lời giải:
nH2 = 1/2 = 0,5mol.
nO2 = 8/32 = 0,25 mol.
nN2 = 3,5/28 = 0,125 mol.
nCO2 = 33/44 = 0,75 mol.
Sơ đồ biểu thị về tỉ lệ thể tích cúa các khí.
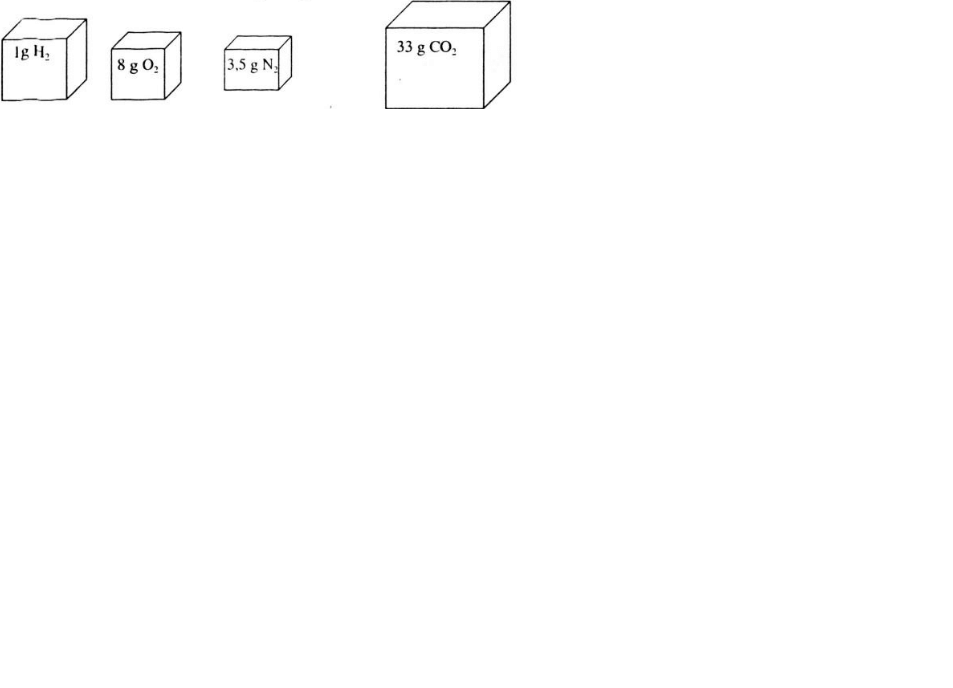
Tỉ lệ số mol các chất khí cũng chính là tỉ lệ về thể tích các khí nên thể tích khí VCO2 > VH2 > VO2 > VN2.
