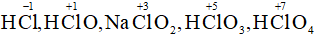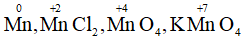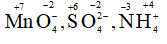- GIẢI BÀI TẬP HÓA 10 SÁCH GIÁO KHOA – CHƯƠNG I – BÀI 1 THÀNH PHẦN NGUYÊN TỬ
- GIẢI BÀI TẬP HÓA 10 SÁCH GIÁO KHOA – CHƯƠNG I – BÀI 2 HẠT NHÂN NGUYÊN TỬ – NGUYÊN TỐ HÓA HỌC – ĐỒNG VỊ
- GIẢI BÀI TẬP HÓA 10 SÁCH GIÁO KHOA – CHƯƠNG I – BÀI 3 LUYỆN TẬP: THÀNH PHẦN NGUYÊN TỬ
- GIẢI BÀI TẬP HÓA 10 SÁCH GIÁO KHOA – CHƯƠNG I – BÀI 4 CẤU TẠO NGUYÊN TỬ
- GIẢI BÀI TẬP HÓA 10 SÁCH GIÁO KHOA – CHƯƠNG I – BÀI 5 CẤU HÌNH ELECTRON
- GIẢI BÀI TẬP HÓA 10 SÁCH GIÁO KHOA – CHƯƠNG I – BÀI 6 LUYỆN TẬP: CẤU TẠO VỎ NGUYÊN TỬ
- GIẢI BÀI TẬP HÓA 10 SÁCH GIÁO KHOA – CHƯƠNG II – BÀI 7 BẢNG TUẦN HOÀN NGUYÊN TỐ HÓA HỌC
- GIẢI BÀI TẬP HÓA 10 SÁCH GIÁO KHOA – CHƯƠNG II – BÀI 11: LUYỆN TẬP : BẢNG TUẦN HOÀN, SỰ BIẾN ĐỔI TUẦN HOÀN CẤU HÌNH ELECTRON NGUYÊN TỬ VÀ TÍNH CHẤT CỦA CÁC NGUYÊN TỐ HÓA HỌC
- GIẢI BÀI TẬP HÓA 10 SÁCH GIÁO KHOA – CHƯƠNG II – BÀI 8 SỰ BIẾN ĐỔI TUẦN HOÀN CẤU HÌNH ELECTRON NGUYÊN TỬ CỦA CÁC NGUYÊN TỐ HÓA HỌC
- GIẢI BÀI TẬP HÓA 10 SÁCH GIÁO KHOA – CHƯƠNG II – BÀI 10 Ý NGHĨA CỦA BẢNG TUẦN HOÀN NGUYÊN TỐ HÓA HỌC
- GIẢI BÀI TẬP HÓA 10 SÁCH GIÁO KHOA – CHƯƠNG III – BÀI 12 LIÊN KẾT ION – TINH THỂ ION
- GIẢI BÀI TẬP HÓA 10 SÁCH GIÁO KHOA – CHƯƠNG III – BÀI 13 LIÊN KẾT CỘNG HÓA TRỊ
- GIẢI BÀI TẬP HÓA 10 SÁCH GIÁO KHOA – CHƯƠNG III – BÀI 14 TINH THỂ NGUYÊN TỬ VÀ TINH THỂ PHÂN TỬ
- GIẢI BÀI TẬP HÓA 10 SÁCH GIÁO KHOA – CHƯƠNG III – BÀI 15 HÓA TRỊ VÀ SỐ OXI HÓA
- GIẢI BÀI TẬP HÓA 10 SÁCH GIÁO KHOA – CHƯƠNG IV – BÀI 17 PHẢN ỨNG OXI HÓA KHỬ
- GIẢI BÀI TẬP HÓA 10 SÁCH GIÁO KHOA – CHƯƠNG III – BÀI 16 LUYỆN TẬP: LIÊN KẾT HÓA HỌC
- GIẢI BÀI TẬP HÓA 10 SÁCH GIÁO KHOA – CHƯƠNG IV – BÀI 18 PHÂN LOẠI PHẢN ỨNG TRONG HÓA HỌC VÔ CƠ
- GIẢI BÀI TẬP HÓA 10 SÁCH GIÁO KHOA – CHƯƠNG IV – BÀI 19 LUYỆN TẬP: PHẢN ỨNG OXI HÓA – KHỬ
- GIẢI BÀI TẬP HÓA 10 SÁCH GIÁO KHOA – CHƯƠNG V – BÀI 21 KHÁI QUÁT VỀ HALOGEN
- GIẢI BÀI TẬP HÓA 10 SÁCH GIÁO KHOA – CHƯƠNG V – BÀI 22 CLO
- GIẢI BÀI TẬP HÓA 10 SÁCH GIÁO KHOA – CHƯƠNG IV – BÀI 20 BÀI THỰC HÀNH SỐ 1- PHẢN ỨNG OXI HÓA KHỬ
- GIẢI BÀI TẬP HÓA 10 SÁCH GIÁO KHOA – CHƯƠNG V – BÀI 23 HIDRO CLORUA – AXIT CLOHIDRIC VÀ MUỐI CLORUA
- GIẢI BÀI TẬP HÓA 10 SÁCH GIÁO KHOA – CHƯƠNG V – BÀI 24 SƠ LƯỢC VỀ HỢP CHẤT CÓ OXI CỦA CLO
- GIẢI BÀI TẬP HÓA 10 SÁCH GIÁO KHOA – CHƯƠNG V – BÀI 25 FLO – BROM – IOT
- GIẢI BÀI TẬP HÓA 10 SÁCH GIÁO KHOA – CHƯƠNG V – BÀI 26 LUYỆN TẬP NHÓM HALOGEN
- GIẢI BÀI TẬP HÓA 10 SÁCH GIÁO KHOA – CHƯƠNG V – BÀI 27 BÀI THỰC HÀNH 2: TÍNH CHẤT HÓA HỌC KHÍ CLO VÀ HỢP CHẤT CỦA CLO
- GIẢI BÀI TẬP HÓA 10 SÁCH GIÁO KHOA – CHƯƠNG VI – BÀI 29 OXI – OZON
- GIẢI BÀI TẬP HÓA 10 SÁCH GIÁO KHOA – CHƯƠNG VI – BÀI 30 LƯU HUỲNH
- GIẢI BÀI TẬP HÓA 10 SÁCH GIÁO KHOA – CHƯƠNG V – BÀI 28 BÀI THỰC HÀNH SỐ 3: TÍNH CHẤT HÍA HỌC CỦA BROM VÀ IOT
- GIẢI BÀI TẬP HÓA 10 SÁCH GIÁO KHOA – CHƯƠNG VI – BÀI 31: BÀI THỰC HÀNH SỐ 4. TÍNH CHẤT CỦA OXI, LƯU HUỲNH
- GIẢI BÀI TẬP HÓA 10 SÁCH GIÁO KHOA – CHƯƠNG VI – BÀI 32 HIDRO SUNFUA – LƯU HUỲNH DIOXIT – LƯU HUỲNH TRIOXIT
- GIẢI BÀI TẬP HÓA 10 SÁCH GIÁO KHOA – CHƯƠNG VI – BÀI 33 AXIT SUNFURIC – MUỐI SUNFAT
- GIẢI BÀI TẬP HÓA 10 SÁCH GIÁO KHOA – CHƯƠNG VI – BÀI 34 LUYỆN TẬP : OXI VÀ LƯU HUỲNH
- GIẢI BÀI TẬP HÓA 10 SÁCH GIÁO KHOA – CHƯƠNG VI – BÀI 35 BÀI THỰC HÀNH SỐ 5. TÍNH CHẤT CÁC HỢP CHẤT CỦA LƯU HUỲNH
- GIẢI BÀI TẬP HÓA 10 SÁCH GIÁO KHOA – CHƯƠNG VII – BÀI 36 TỐC ĐỘ PHẢN ỨNG HÓA HỌC
- GIẢI BÀI TẬP HÓA 10 SÁCH GIÁO KHOA – CHƯƠNG VII – BÀI 37 BÀI THỰC HÀNH SỐ 6. TỐC ĐỘ PHẢN ỨNG HÓA HỌC
- GIẢI BÀI TẬP HÓA 10 SÁCH GIÁO KHOA – CHƯƠNG VII – BÀI 38 CÂN BẰNG HÓA HỌC
- GIẢI BÀI TẬP HÓA 10 SÁCH GIÁO KHOA – CHƯƠNG VII – BÀI 39 LUYỆN TẬP : TỐC ĐỘ PHẢN ỨNG HÓA HOC
Bài 15: Hóa trị và số oxi hóa
Bài 1 (trang 74 SGK Hóa 10): Số oxi hóa của nitơ trong NH4+, NO2– và HNO3 lần lượt là:
A. +5, – 3, +3.
B. -3, +3, +5.
C. +3, -3, +5.
D. +3, +5, -3.
Chọn đáp án đúng
Lời giải:
B đúng.
Gọi số oxi hóa của N trong các hợp chất là x
Ta có NH4+: x + 4 = 1 ⇒ x = -3 ⇒ Số oxi hóa của N trong NH4+ là -3
NO2–: x + 2.(-2) = -1 ⇒ x = 3 ⇒ số oxi hóa của N trong NO2– là +3
HNO3: 1 + x + 3.(-2) = 0 ⇒ x = 5 ⇒ số oxi hóa của N tròng HNO3 là +5
Bài 2 (trang 74 SGK Hóa 10): Số oxi hóa của Mn, Fe trong Fe3+, S trong SO3, P trong PO43- lần lượt là:
A. 0, +3, +6, +5.
B. 0, +3, +5, +6.
C. +3, + 5, 0, +6.
D. +5, +6, +3, 0.
Chọn đáp án đúng.
Lời giải:
A đúng.
Mn là đơn chất nên có số oxi hóa 0
Fe3+ có số oxi hóa +3
SO3: x + 3.(-2) = 0 ⇒ x = 6 ⇒ số oxi hóa của S là +6
PO43-: x + 4.(-2) = -3 ⇒ x = 5 ⇒ số oxi hóa của P là +5
Bài 3 (trang 74 SGK Hóa 10): Hãy cho biết điện hóa trị của các nguyên tử trong các hợp chất sau đây: CsCl, Na2O, BaO, BaCl2, Al2O3.
Lời giải:
Cs = 1+; Cl = 1–; Na = 1+; O = 2–; Ba = 2+; O = 2–
Ba = 2+; Cl = 1–; Al = 3+; O = 2–
Bài 4 (trang 74 SGK Hóa 10): Hãy xác định cộng hóa trị của các nguyên tố trong các hợp chất sau đây: H2O, CH4, HCl, NH3.
Lời giải:
Cộng hóa trị của các nguyên tố trong hợp chất:
| H2O | CH4 | HCl | NH3 | |
| Cộng hóa trị | H có cộng hóa trị là 1. O có cộng hóa trị là 2 | C có cộng hóa trị là 4. H có cộng hóa trị là 1 | H và Cl đều có cộng hóa trị là 1 | N có cộng hóa trị là 3. H là cộng hóa trị là 1 |
Bài 5 (trang 74 SGK Hóa 10): Xác định số oxi hóa của các nguyên tố trong các phân tử và ion sau: CO2, H2O, SO3, NH3, NO, NO2, Na+, Cu2+, Fe2+, Fe3+, Al3+.
Lời giải:
O có số oxi hóa -2, H có số oxi hóa + 1
⇒ Số oxi hóa của các nguyên tố trong các phân tử và ion là:
CO2: x + 2.(-2) = 0 ⇒ x = 4 ⇒ C có số oxi hóa +4 trong CO2
H2O: H có số oxi hóa +1, O có số oxi hóa -2.
SO3: x + 3.(-2) = 0 ⇒ x = 6 ⇒ S có số oxi hóa +6 trong SO3
NH3: x + 3.1 = 0 ⇒ x = -3 ⇒ N có số oxi hóa -3 trong NH3
NO: x + 1.(-2) = 0 ⇒ x = 2 ⇒ N có số oxi hóa +2 trong NO
NO2: x + 2.(-2) = 0 ⇒ x = 4 ⇒ N có số oxi hóa +4 trong NO2
Cu2+ có số oxi hóa là +2.
Na+ có số oxi hóa là +1.
Fe2+ có số oxi hóa là +2.
Fe3+ có số oxi hóa là +3.
Al3+ có số oxi hóa là +3.
Bài 6 (trang 74 SGK Hóa 10): Viết công thức phân tử của những chất, trong đó S lần lượt có số oxi hóa -2, 0, +4, +6.
Lời giải:
Công thức phân tử của những chất trong đó S có số oxi hóa -2, 0, +4, +6 lần lượt là : H2S, S, SO2, SO3.
Bài 7 (trang 74 SGK Hóa 10): Xác định số oxi hóa của các nguyên tố trong các hợp chất, đơn chất và ion sau:
a) H2S, S, H2SO3, H2SO4.
b) HCl, HClO, NaClO2, HClO3, HClO4.
c) Mn, MnCl2, MnO2, KMnO4.
d) MnO4–, SO42-, NH4+.
Lời giải:
a) O có số oxi hóa -2, H có số oxi hóa +1 trong các hợp chất.
⇒ Số oxi hóa của S trong các chất :
H2S: 1.2 + x = 0 ⇒ x = -2 ⇒ số oxi hóa của S là -2 trong H2S
S đơn chất có số oxi hóa 0
H2SO3: 1.2 + x + 3.(-2) = 0 ⇒ x= 4 ⇒ S có số oxi hóa +4 trong H2SO3
H2SO4: 1.2 + x + 4.(-2) = 0 ⇒ x = 6 ⇒ S có số oxi hóa +6 trong H2SO4
b)Tương tự số oxi hóa của Cl trong các hợp chất là:
c) Tương tự số oxi hóa của Mn trong các chất:
d) Tương tự số oxi hóa của Mn trong các chất