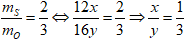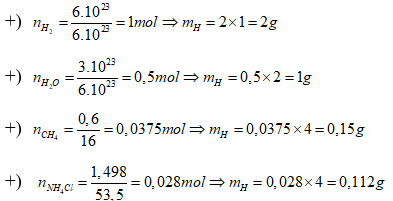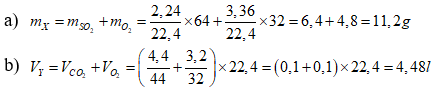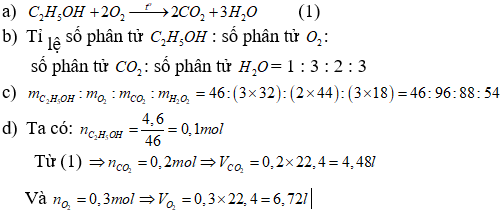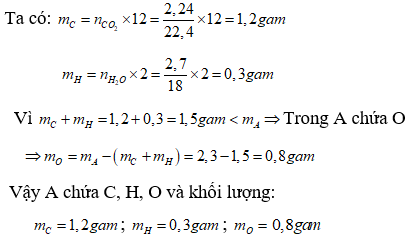- Đề kiểm tra 15 phút Hóa học 8 Chương 1 (Đề 1)
- Đề kiểm tra 15 phút Hóa học 8 Chương 1 (Đề 2)
- Đề kiểm tra 15 phút Hóa học 8 Chương 1 (Đề 3)
- Đề kiểm tra 15 phút Hóa học 8 Chương 1 (Đề 4)
- Đề kiểm tra 15 phút Hóa học 8 Chương 1 (Đề 5)
- Đề kiểm tra 1 tiết Hóa học 8 Chương 1 (Đề 1)
- Đề kiểm tra 1 tiết Hóa học 8 Chương 1 (Đề 2)
- Đề kiểm tra 15 phút Hóa học 8 Chương 2 (Đề 1)
- Đề kiểm tra 1 tiết Hóa học 8 Chương 1 (Đề 3)
- Đề kiểm tra 1 tiết Hóa học 8 Chương 1 (Đề 4)
- Đề kiểm tra 15 phút Hóa học 8 Chương 2 (Đề 2)
- Đề kiểm tra 15 phút Hóa học 8 Chương 2 (Đề 3)
- Đề kiểm tra 15 phút Hóa học 8 Chương 2 (Đề 4)
- Đề kiểm tra 15 phút Hóa học 8 Chương 2 (Đề 5)
- Đề kiểm tra 1 tiết Hóa học 8 Chương 2 (Đề 1)
- Đề kiểm tra 1 tiết Hóa học 8 Chương 2 (Đề 2)
- Đề kiểm tra 1 tiết Hóa học 8 Chương 2 (Đề 4)
- Đề kiểm tra 1 tiết Hóa học 8 Chương 2 (Đề 5)
- Đề kiểm tra 15 phút Hóa học 8 Chương 3 (Đề 1)
- Đề kiểm tra 15 phút Hóa học 8 Chương 3 (Đề 2)
- Đề kiểm tra 15 phút Hóa học 8 Chương 3 (Đề 3)
- Đề kiểm tra 15 phút Hóa học 8 Chương 3 (Đề 4)
- Đề kiểm tra 15 phút Hóa học 8 Chương 3 (Đề 5)
- Đề kiểm tra 1 tiết Hóa học 8 Chương 3 (Đề 1)
- Đề kiểm tra 1 tiết Hóa học 8 Chương 3 (Đề 2)
- Đề kiểm tra 1 tiết Hóa học 8 Chương 3 (Đề 3)
- Đề kiểm tra 1 tiết Hóa học 8 Chương 3 (Đề 4)
- Đề kiểm tra Học kì 1 Hóa học lớp 8 (Đề 1)
- Đề kiểm tra Học kì 1 Hóa học lớp 8 (Đề 2)
- Đề kiểm tra Học kì 1 Hóa học lớp 8 (Đề 4)
- Đề thi hóa 8 học kì 1 (Đề 1)
- Đề thi hóa 8 học kì 1 (Đề 2)
- Đề thi hóa 8 học kì 1 (Đề 3)
- Đề thi hóa 8 học kì 1 (Đề 4)
- Đề kiểm tra 15 phút Hóa học 8 Chương 4 (Đề 1)
- Đề kiểm tra 15 phút Hóa học 8 Chương 4 (Đề 2)
- Đề kiểm tra 15 phút Hóa học 8 Chương 4 (Đề 3)
- Đề kiểm tra 15 phút Hóa học 8 Chương 4 (Đề 4)
- Đề kiểm tra 15 phút Hóa học 8 Chương 4 (Đề 5)
- Đề kiểm tra 1 tiết Hóa học 8 Chương 4 (Đề 1)
- Đề kiểm tra 1 tiết Hóa học 8 Chương 4 (Đề 2)
- Đề kiểm tra 1 tiết Hóa học 8 Chương 4 (Đề 3)
- Đề kiểm tra 1 tiết Hóa học 8 Chương 4 (Đề 4)
- Đề kiểm tra 1 tiết Hóa học 8 Chương 4 (Đề 5)
- Đề kiểm tra 15 phút Hóa học 8 Chương 5 (Đề 1)
- Đề kiểm tra 15 phút Hóa học 8 Chương 5 (Đề 2)
- Đề kiểm tra 15 phút Hóa học 8 Chương 5 (Đề 3)
- Đề kiểm tra 15 phút Hóa học 8 Chương 5 (Đề 4)
- Đề kiểm tra 15 phút Hóa học 8 Chương 5 (Đề 5)
- Đề kiểm tra 1 tiết Hóa học 8 Chương 5 (Đề 1)
- Đề kiểm tra 1 tiết Hóa học 8 Chương 5 (Đề 3)
- Đề kiểm tra 1 tiết Hóa học 8 Chương 5 (Đề 4)
- Đề kiểm tra 15 phút Hóa học 8 Chương 6 (Đề 1)
- Đề kiểm tra 15 phút Hóa học 8 Chương 6 (Đề 2)
- Đề kiểm tra 15 phút Hóa học 8 Chương 6 (Đề 3)
- Đề kiểm tra 15 phút Hóa học 8 Chương 6 (Đề 4)
- Đề kiểm tra 15 phút Hóa học 8 Chương 6 (Đề 5)
- Đề kiểm tra 1 tiết Hóa học 8 Chương 6 (Đề 1)
- Đề kiểm tra 1 tiết Hóa học 8 Chương 6 (Đề 2)
- Đề kiểm tra 1 tiết Hóa học 8 Chương 6 (Đề 3)
- Đề kiểm tra 1 tiết Hóa học 8 Chương 6 (Đề 4)
- Đề thi hóa 8 học kì 2 (Đề 1)
- Đề thi hóa 8 học kì 2 (Đề 2)
- Đề thi hóa 8 học kì 2 (Đề 3)
- Đề thi hóa 8 học kì 2 (Đề 4)
- Đề thi hóa 8 học kì 2 (Đề 5)
Đề kiểm tra 1 tiết Hóa học 8 Chương 3 (Đề 4)
Đề kiểm tra 1 tiết Hóa học 8 Chương 3 (Đề 4)
Câu 1. Một oxit lưu huỳnh trong đó có thành phần gồm 2 phần khối lượng nguyên tố S và 3 phần khối lượng nguyên tố O (mS/mO=2/3). Xác định công thức lưu huỳnh đó.
Câu 2. Trường hợp nào sau đây chưa khối lượng nguyên tử hidro lớn nhất
a) 6.10^23 phân tử H2
b) b) phân tử H2O
c) 0,6 gam CH4
d) 1,498 gam NH4Cl
Câu 3.
a) Tính khối lượng của một hỗn hợp khí (X) ở đktc gồm 2,24l SO2 và 3,36 lít O2
b) Tính thể tích ở đktc của một hỗn hợp khí (Y) gồm 4,4g CO2 vầ 3,2g O2
Câu 4. Phản ứng hóa học xảy ra khi đèn cồn cháy (đèn cồn trong phòng thí nghiệm) là:
Rượu etylic C2H5OH +oxi −to→ khí cacbonic (CO2) +nước
a) Lập phương trình hóa học của phản ứng.
b) Cho biết tỉ lệ số phân tử của các chất trong phản ứng hóa học.
c) Tính tỉ lệ về khối lượng giữa các chất trong phản ứng hóa học.
d) Tính thể tích oxi cần thiết để đốt cháy hết 4,6 gam rượu etylic và thể tích khí cacbonic tạo thành ở đktc.
Câu 5. Đốt cháy hoàn toàn 2,3 gam X bằng khí oxi, sau phản ứng thu được 2,24 lít CO2 đktc và 2,7 gam nước. Hỏi A được cấu tạo từ những nguyên tố hóa học nào. Tính khối lượng từng nguyên tố trong 2,3 gam X.
Đáp án và hướng dẫn giải Đề kiểm tra 1 tiết Hóa học 8 Chương 3 (Đề 4)
Câu 1. Theo đề bài ta có
Vậy công thức hóa học của oxit lưu huỳnh : SO2
Câu 2. Ta có
Câu 3.
Câu 4.
Câu 5. Vì A cháy sinh ra CO2 và H2O nên A chứa C, H, và có thể có O.