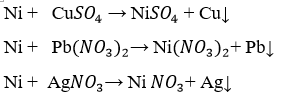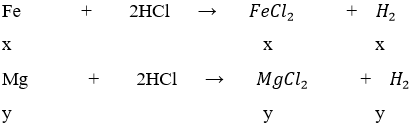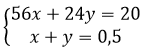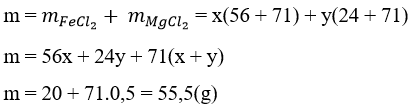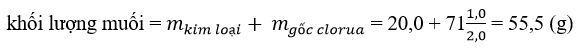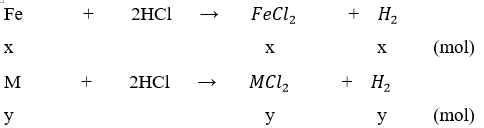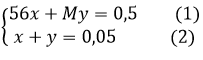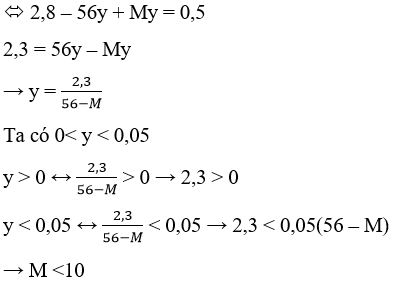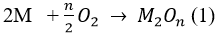- GIẢI BÀI TẬP HÓA 12 SÁCH GIÁO KHOA CHƯƠNG I – BÀI 1: Este
- GIẢI BÀI TẬP HÓA 12 SÁCH GIÁO KHOA CHƯƠNG I – BÀI 2: Lipit
- GIẢI BÀI TẬP HÓA 12 SÁCH GIÁO KHOA CHƯƠNG I – BÀI 3: Khái niệm về xà phòng và chất giặt rửa tổng hợp
- GIẢI BÀI TẬP HÓA 12 SÁCH GIÁO KHOA CHƯƠNG I – BÀI 4: Luyện tập: Este và chất béo
- GIẢI BÀI TẬP HÓA 12 SÁCH GIÁO KHOA CHƯƠNG II – BÀI 5: Glucozơ
- GIẢI BÀI TẬP HÓA 12 SÁCH GIÁO KHOA CHƯƠNG II – BÀI 6: Saccarozơ, tinh bột và xenlulozơ
- GIẢI BÀI TẬP HÓA 12 SÁCH GIÁO KHOA CHƯƠNG II – BÀI 7: Luyện tập: Cấu tạo và tính chất của cacbohiđrat
- GIẢI BÀI TẬP HÓA 12 SÁCH GIÁO KHOA CHƯƠNG II – BÀI 8: Thực hành: Điều chế tính chất hóa học của este và cacbohiđrat
- GIẢI BÀI TẬP HÓA 12 SÁCH GIÁO KHOA CHƯƠNG III – BÀI 9: Amin
- GIẢI BÀI TẬP HÓA 12 SÁCH GIÁO KHOA CHƯƠNG III – BÀI 10: Amino axit
- GIẢI BÀI TẬP HÓA 12 SÁCH GIÁO KHOA CHƯƠNG III – BÀI 11: Peptit và protein
- GIẢI BÀI TẬP HÓA 12 SÁCH GIÁO KHOA CHƯƠNG III – BÀI 12: Luyện tập: Cấu tạo và tính chất của amin, amino axit và protein
- GIẢI BÀI TẬP HÓA 12 SÁCH GIÁO KHOA CHƯƠNG IV – BÀI 13: Đại cương về polime
- GIẢI BÀI TẬP HÓA 12 SÁCH GIÁO KHOA CHƯƠNG IV – BÀI 14: Vật liệu polime
- GIẢI BÀI TẬP HÓA 12 SÁCH GIÁO KHOA CHƯƠNG IV – BÀI 15: Luyện tập: Polime và vật liệu polime
- GIẢI BÀI TẬP HÓA 12 SÁCH GIÁO KHOA CHƯƠNG IV – BÀI 16: Thực hành: Một số tính chất của protein và vật liệu polime
- GIẢI BÀI TẬP HÓA 12 SÁCH GIÁO KHOA CHƯƠNG V – BÀI 17: Vị trí của kim loại trong bảng tuần hoàn và cấu tạo của kim loại
- GIẢI BÀI TẬP HÓA 12 SÁCH GIÁO KHOA CHƯƠNG V – BÀI 18: Tính chất của kim loại. Dãy điện hóa của kim loại
- GIẢI BÀI TẬP HÓA 12 SÁCH GIÁO KHOA CHƯƠNG V – BÀI 19: Hợp kim
- GIẢI BÀI TẬP HÓA 12 SÁCH GIÁO KHOA CHƯƠNG V – BÀI 20: Sự ăn mòn kim loại
- GIẢI BÀI TẬP HÓA 12 SÁCH GIÁO KHOA CHƯƠNG V – BÀI 21: Điều chế kim loại
- GIẢI BÀI TẬP HÓA 12 SÁCH GIÁO KHOA CHƯƠNG V – BÀI 22: Luyện tập: Tính chất của kim loại
- GIẢI BÀI TẬP HÓA 12 SÁCH GIÁO KHOA CHƯƠNG V – BÀI 23: Luyện tâp: Điều chế kim loại và sự ăn mòn kim loại
- GIẢI BÀI TẬP HÓA 12 SÁCH GIÁO KHOA CHƯƠNG V – BÀI 24: Thực hành: Tính chất, điều chế kim loại, sự ăn mòn kim loại
- GIẢI BÀI TẬP HÓA 12 SÁCH GIÁO KHOA CHƯƠNG VI – BÀI 25: Kim loại kiềm và hợp chất quan trọng của kim loại kiềm
- GIẢI BÀI TẬP HÓA 12 SÁCH GIÁO KHOA CHƯƠNG VI – BÀI 26: Kim loại kiềm thổ
- GIẢI BÀI TẬP HÓA 12 SÁCH GIÁO KHOA CHƯƠNG VI – BÀI 27: Nhôm và hợp chất của nhôm
- GIẢI BÀI TẬP HÓA 12 SÁCH GIÁO KHOA CHƯƠNG VI – BÀI 28: Luyện tập: Tính chất của kim loại kiềm, kim loại kiềm thổ và hợp chất của chúng
- GIẢI BÀI TẬP HÓA 12 SÁCH GIÁO KHOA CHƯƠNG VI – BÀI 29: Luyện tập: Tính chất của nhôm và hợp chất của nhôm
- GIẢI BÀI TẬP HÓA 12 SÁCH GIÁO KHOA CHƯƠNG VI – BÀI 30: Thực hành: Tính chất của natri, magie, nhôm và hợp chất của chúng
- GIẢI BÀI TẬP HÓA 12 SÁCH GIÁO KHOA CHƯƠNG VI – BÀI 31: Sắt
- GIẢI BÀI TẬP HÓA 12 SÁCH GIÁO KHOA CHƯƠNG VI – BÀI 32: Hợp chất của sắt
- GIẢI BÀI TẬP HÓA 12 SÁCH GIÁO KHOA CHƯƠNG VI – BÀI 33: Hợp kim của sắt
- GIẢI BÀI TẬP HÓA 12 SÁCH GIÁO KHOA CHƯƠNG VII – BÀI 34: Crom và hợp chất của crom
- GIẢI BÀI TẬP HÓA 12 SÁCH GIÁO KHOA CHƯƠNG VII – BÀI 35: Đồng và hợp chất của đồng
- GIẢI BÀI TẬP HÓA 12 SÁCH GIÁO KHOA CHƯƠNG VII – BÀI 36: Sơ lược về niken, kẽm, chì, thiếc
- GIẢI BÀI TẬP HÓA 12 SÁCH GIÁO KHOA CHƯƠNG VII – BÀI 37: Luyện tập: Tính chất hóa học của sắt và hợp chất của sắt
- GIẢI BÀI TẬP HÓA 12 SÁCH GIÁO KHOA CHƯƠNG VII – BÀI 38: Luyện tập: Tính chất hóa học của crom, đồng và hợp chất của chúng
- GIẢI BÀI TẬP HÓA 12 SÁCH GIÁO KHOA CHƯƠNG VII – BÀI 39: Thực hành: Tính chất hóa học của sắt, đồng và nhưng hợp chất của sắt, crom
- GIẢI BÀI TẬP HÓA 12 SÁCH GIÁO KHOA CHƯƠNG VIII – BÀI 40: Nhận biết một số ion trong dung dịch
- GIẢI BÀI TẬP HÓA 12 SÁCH GIÁO KHOA CHƯƠNG VIII – BÀI 41: Nhận biết một số chất khí
- GIẢI BÀI TẬP HÓA 12 SÁCH GIÁO KHOA CHƯƠNG VIII – BÀI 42: Luyện tập: Nhận biết một số chất vô cơ
- GIẢI BÀI TẬP HÓA 12 SÁCH GIÁO KHOA CHƯƠNG IX – BÀI 43: Hóa học và vấn đề phát triển kinh tế
- GIẢI BÀI TẬP HÓA 12 SÁCH GIÁO KHOA CHƯƠNG IX – BÀI 44: Hóa học và vấn đề xã hội
- Bài 45: hóa học và các vấn đề môi trường Giải bài tập hóa 12
Bài 22: Luyện tập: Tính chất của kim loại
Bài 1 (trang 100 SGK Hóa 12):
Có 4 ion là Ca2+, Al3+, Fe2+, Fe3+. Ion có số electron lớp ngoài cùng nhiều nhất là :
A. Fe3+.
B. Fe2+.
C. Al3+.
D. Ca2+.
Lời giải:
Đáp án B.
Bài 2 (trang 100 SGK Hóa 12):
Kim loại có tính chất vật lý chung là dẫn điện, dẫn nhiệt, dẻo và có ánh kim. Nguyên nhân của những tính chất vật lý chung là :
A. trong tinh thể kim loại có nhiều electron độc thân.
B. trong tinh thể kim loại có các ion dương chuyển động tự do.
C. trong tinh thể kim loại có các electron chuyển động tự do.
D. trong tinh thể kim loại có nhiều ion dương kim loại.
Lời giải:
Đáp án C.
Bài 3 (trang 100 SGK Hóa 12):
Kim loại khác nhau có độ dẫn điện, dẫn nhiệt khác nhau, sự khác nhau đó được quyết định bởi đặc điểm nào sau đây?
A. có khối lượng riêng khác nhau.
B. có kiểu mạng tinh thể khác nhau.
C. có mật độ electron tự do khác nhau.
D. có mật độ ion dương khác nhau.
Lời giải:
Đáp án C.
Bài 4 (trang 100 SGK Hóa 12):
Ngâm một lá kim loại Ni trong những dung dịch muối sau: MgSO4, NaCl, CuSO4, AlCl3, ZnCl2, Pb(NO3)2, AgNO3. Hãy cho biết muối nào có phản ứng với Ni. Giải thích và viết phương trình hoá học.
Lời giải:
Niken có thể phản ứng được với các dung dịch muối sau đây:
Bài 5 (trang 101 SGK Hóa 12): Để làm sạch một mẫu thủy ngân có lẫn tạp chất là kẽm, thiếc, chì người ta khuấy mẫu thủy ngân này trong dung dịch HgSO4 dư.
a. Hãy giải thích phương pháp làm sạch và viết phương trình hóa học.
b. Nếu bạc có lẫn tạp chất là kim loại nói trên, hãy làm cách nào để loại bỏ được tạp chất? Viết phương trình hóa học.
Lời giải:
a, Khuấy mẫu thủy ngân trong dung dịch Hg4 có các phản ứng
HgSO4 + Zn → Zn4 + Hg
HgSO4 + Sn → Sn4 + Hg
HgSO4 + Pb → Pb4 + Hg
Như vậy các tạp chất Zn, Sn, Pb bị hòa tan hết. Lọc lấy thu thủy ngân tinh khiết.
b, Nếu bạc có lẫn các kim loại nói trên cho hỗn hợp vào dung dịch AgNO3. Sẽ có các phản úng xảy ra:
Zn + 2AgNO3 → Zn(NO3)2 + 2Ag↓
Sn + 2AgNO3 → Sn(NO3)2 + 2Ag↓
Pb + 2AgNO3 → Pb(NO3)2 + 2Ag↓
Khi đó các kim loại bị hòa tan hết trong dung dịch AgNO3 lọc lấy kết tủa thu được Ag tinh khiết
Bài 5 (trang 101 SGK Hóa 12):
Để làm sạch một mẫu thủy ngân có lẫn tạp chất là kẽm, thiếc, chì người ta khuấy mẫu thủy ngân này trong dung dịch HgSO4 dư.
a. Hãy giải thích phương pháp làm sạch và viết phương trình hóa học.
b. Nếu bạc có lẫn tạp chất là kim loại nói trên, hãy làm cách nào để loại bỏ được tạp chất? Viết phương trình hóa học.
Lời giải:
a, Khuấy mẫu thủy ngân trong dung dịch Hg4 có các phản ứng
HgSO4 + Zn → Zn4 + Hg
HgSO4 + Sn → Sn4 + Hg
HgSO4 + Pb → Pb4 + Hg
Như vậy các tạp chất Zn, Sn, Pb bị hòa tan hết. Lọc lấy thu thủy ngân tinh khiết.
b, Nếu bạc có lẫn các kim loại nói trên cho hỗn hợp vào dung dịch AgNO3. Sẽ có các phản úng xảy ra:
Zn + 2AgNO3 → Zn(NO3)2 + 2Ag↓
Sn + 2AgNO3 → Sn(NO3)2 + 2Ag↓
Pb + 2AgNO3 → Pb(NO3)2 + 2Ag↓
Khi đó các kim loại bị hòa tan hết trong dung dịch AgNO3 lọc lấy kết tủa thu được Ag tinh khiết
Bài 6 (trang 101 SGK Hóa 12):
Hòa tan hoàn toàn 20 gam hỗn hợp Fe và Mg trong dung dịch HCl thu 1 gam khí H2. Khi cô cạn dung dịch thu được bao nhiêu gam muối khan?
A. 54,5(g)
B. 55,5(g)
C. 56,5(g)
D. 57,5(g)
Lời giải:
Đáp án B.
• Cách 1:
gọi x, y lần lượt là số mol của Fe và Mg trong hỗn hợp
số mol H2 là nH2 = 1/2 = 0,5 (mol)
theo bài ra ta có hệ phương trình
khối lượng muối khan là :
• Cách 2:
Bài 7 (trang 101 SGK Hóa 12):
Hòa tan hoàn toàn 0,5 gam Fe và một kim loại hóa trị II trong dung dịch HCl thu được 1,12 lít khí H2 đktc. Kim loại hóa trị II đó là kim loại nào sau đây.
A. Mg.
B. Ca.
C. Zn.
D. Be.
Lời giải:
Đáp án D.
gọi x, y lần lượt là số mol của Fe và M trong hỗn hợp
số mol H2 là nH2 = 1,12/22,4 = 0,05 (mol)
theo bài ra ta có hệ phương trình
từ (2) → x= 0,05 – y
thay vào (1) ta được 56(0,05 – y) + My = 0,5
Bài 8 (trang 101 SGK Hóa 12):
Cho 16,2 gam kim loại M có hóa trị n tác dụng với 0,15 mol O2. Chất rắn thu được sau phản ứng đem hòa tan vào dung dịch HCl dư thấy thoát ra 13,44 lít khí H2đktc. Kim loại M là kim loại nào sau đây?
A. Fe.
B. Al.
C. Ca.
D. Mg.
Lời giải:
Đáp án B.
Chất rắn sau phản ứng hòa tan trong HCl thấy có khí thoát ra chứng ở có M dư
Bài 9 (trang 101 SGK Hóa 12):
Có 5 mẫu kim loại là Mg, Al, Ba, Fe, Ag. Nếu chỉ dùng thêm dung dịch H2SO4 thì có thể nhận biết được những mẫu kim loại nào ?
A. Mg, Ba, Ag.
B. Mg, Ba, Al.
C. Mg, Ba, Al, Fe.
D. Cả 5 mẫu kim loại.
Lời giải:
Đáp án D.
Bài 10 (trang 101 SGK Hóa 12):
Cho bột đồng vào dung dịch hỗn hợp gồm Fe(NO3)3 và AgNO3sau phản ứng kết thúc thu được chất rắn A và dung dịch B. Viết PTHH của các phản ứng xảy ra. Cho biết A, B gồm những chất gì? Biết rằng :
Tính oxi hóa : Ag+ > Fe3+ > Cu2+ > Fe2+
Tính khử : Cu > Fe2+ > Ag
Lời giải:
Trường hợp Cu dư:
Cu + 2AgNO3 → Cu(NO3)2+ 2Ag ↓
Cu + Fe(NO3)3→ Cu(NO3)2+ Fe(NO3)2
Rắn A : Ag, Cu dư
Dung dịch B : Cu(NO3)2, Fe(NO3)2