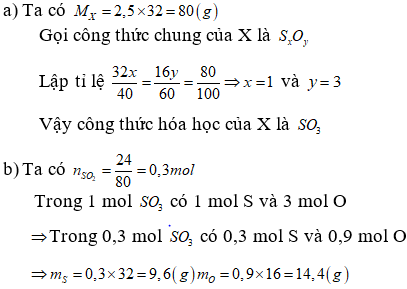- Đề kiểm tra 15 phút Hóa học 8 Chương 1 (Đề 1)
- Đề kiểm tra 15 phút Hóa học 8 Chương 1 (Đề 2)
- Đề kiểm tra 15 phút Hóa học 8 Chương 1 (Đề 3)
- Đề kiểm tra 15 phút Hóa học 8 Chương 1 (Đề 4)
- Đề kiểm tra 15 phút Hóa học 8 Chương 1 (Đề 5)
- Đề kiểm tra 1 tiết Hóa học 8 Chương 1 (Đề 1)
- Đề kiểm tra 1 tiết Hóa học 8 Chương 1 (Đề 2)
- Đề kiểm tra 15 phút Hóa học 8 Chương 2 (Đề 1)
- Đề kiểm tra 1 tiết Hóa học 8 Chương 1 (Đề 3)
- Đề kiểm tra 1 tiết Hóa học 8 Chương 1 (Đề 4)
- Đề kiểm tra 15 phút Hóa học 8 Chương 2 (Đề 2)
- Đề kiểm tra 15 phút Hóa học 8 Chương 2 (Đề 3)
- Đề kiểm tra 15 phút Hóa học 8 Chương 2 (Đề 4)
- Đề kiểm tra 15 phút Hóa học 8 Chương 2 (Đề 5)
- Đề kiểm tra 1 tiết Hóa học 8 Chương 2 (Đề 1)
- Đề kiểm tra 1 tiết Hóa học 8 Chương 2 (Đề 2)
- Đề kiểm tra 1 tiết Hóa học 8 Chương 2 (Đề 4)
- Đề kiểm tra 1 tiết Hóa học 8 Chương 2 (Đề 5)
- Đề kiểm tra 15 phút Hóa học 8 Chương 3 (Đề 1)
- Đề kiểm tra 15 phút Hóa học 8 Chương 3 (Đề 2)
- Đề kiểm tra 15 phút Hóa học 8 Chương 3 (Đề 3)
- Đề kiểm tra 15 phút Hóa học 8 Chương 3 (Đề 4)
- Đề kiểm tra 15 phút Hóa học 8 Chương 3 (Đề 5)
- Đề kiểm tra 1 tiết Hóa học 8 Chương 3 (Đề 1)
- Đề kiểm tra 1 tiết Hóa học 8 Chương 3 (Đề 2)
- Đề kiểm tra 1 tiết Hóa học 8 Chương 3 (Đề 3)
- Đề kiểm tra 1 tiết Hóa học 8 Chương 3 (Đề 4)
- Đề kiểm tra Học kì 1 Hóa học lớp 8 (Đề 1)
- Đề kiểm tra Học kì 1 Hóa học lớp 8 (Đề 2)
- Đề kiểm tra Học kì 1 Hóa học lớp 8 (Đề 4)
- Đề thi hóa 8 học kì 1 (Đề 1)
- Đề thi hóa 8 học kì 1 (Đề 2)
- Đề thi hóa 8 học kì 1 (Đề 3)
- Đề thi hóa 8 học kì 1 (Đề 4)
- Đề kiểm tra 15 phút Hóa học 8 Chương 4 (Đề 1)
- Đề kiểm tra 15 phút Hóa học 8 Chương 4 (Đề 2)
- Đề kiểm tra 15 phút Hóa học 8 Chương 4 (Đề 3)
- Đề kiểm tra 15 phút Hóa học 8 Chương 4 (Đề 4)
- Đề kiểm tra 15 phút Hóa học 8 Chương 4 (Đề 5)
- Đề kiểm tra 1 tiết Hóa học 8 Chương 4 (Đề 1)
- Đề kiểm tra 1 tiết Hóa học 8 Chương 4 (Đề 2)
- Đề kiểm tra 1 tiết Hóa học 8 Chương 4 (Đề 3)
- Đề kiểm tra 1 tiết Hóa học 8 Chương 4 (Đề 4)
- Đề kiểm tra 1 tiết Hóa học 8 Chương 4 (Đề 5)
- Đề kiểm tra 15 phút Hóa học 8 Chương 5 (Đề 1)
- Đề kiểm tra 15 phút Hóa học 8 Chương 5 (Đề 2)
- Đề kiểm tra 15 phút Hóa học 8 Chương 5 (Đề 3)
- Đề kiểm tra 15 phút Hóa học 8 Chương 5 (Đề 4)
- Đề kiểm tra 15 phút Hóa học 8 Chương 5 (Đề 5)
- Đề kiểm tra 1 tiết Hóa học 8 Chương 5 (Đề 1)
- Đề kiểm tra 1 tiết Hóa học 8 Chương 5 (Đề 3)
- Đề kiểm tra 1 tiết Hóa học 8 Chương 5 (Đề 4)
- Đề kiểm tra 15 phút Hóa học 8 Chương 6 (Đề 1)
- Đề kiểm tra 15 phút Hóa học 8 Chương 6 (Đề 2)
- Đề kiểm tra 15 phút Hóa học 8 Chương 6 (Đề 3)
- Đề kiểm tra 15 phút Hóa học 8 Chương 6 (Đề 4)
- Đề kiểm tra 15 phút Hóa học 8 Chương 6 (Đề 5)
- Đề kiểm tra 1 tiết Hóa học 8 Chương 6 (Đề 1)
- Đề kiểm tra 1 tiết Hóa học 8 Chương 6 (Đề 2)
- Đề kiểm tra 1 tiết Hóa học 8 Chương 6 (Đề 3)
- Đề kiểm tra 1 tiết Hóa học 8 Chương 6 (Đề 4)
- Đề thi hóa 8 học kì 2 (Đề 1)
- Đề thi hóa 8 học kì 2 (Đề 2)
- Đề thi hóa 8 học kì 2 (Đề 3)
- Đề thi hóa 8 học kì 2 (Đề 4)
- Đề thi hóa 8 học kì 2 (Đề 5)
Đề kiểm tra 1 tiết Hóa học 8 Chương 3 (Đề 2)
Đề kiểm tra 1 tiết Hóa học 8 Chương 3 (Đề 2)
Câu 1: Trong một bình trộn khí SO2 với SO3 . Khi phân tích người ta thấy có 2,4 gam lưu huỳnh và 2,8 gam oxi. Xác định tỉ số mol SO2 và SO3 trong bình.
Câu 2: Một halogen (X) có tỉ khối hơi đối với khí axetilen ( C2H2) bằng 2,731. Xác định tên gọi của halogen (X)
Câu 3: Lưu huỳnh cháy trong không khí sinh ra khí sunfurơ, theo phản ứng sau:
S + O2 −to→ SO2
Hãy cho biết:
a) Những chất tham gia và tạo thành trong phản ứng trên, chất nào là đơn chất, chất nào là hợp chất? Vì sao?
b) Thể tích khí oxi ở đktc cần dùng để đốt cháy hoàn toàn 2,5 mol nguyên tử lưu huỳnh.
c) Khí sunfurơ nặng hay nhẹ hơn không khí. Hãy giải thích.
Câu 4: Hãy tính:
a) Khối lượng và thể tích của 0,25 mol khí SO2 đktc.
b) Số nguyên tử và thể tích của 10,65 gam khí Cl2 đktc
Câu 5: Một hợp chất X có thành phần phần trăm khối lượng mỗi nguyên tố là : %S=40% và %O=60%
a) Hãy xác định công thức hóa học của X. Biết tỉ khối của X đối với khí oxi là 2,5.
b) Hãy tính khối lượng mỗi nguyên tố có trong 24g hợp chất X.
Đáp án và hướng dẫn giải Đề kiểm tra 1 tiết Hóa học 8 Chương 3 (Đề 2)
Câu 1. Gọi số mol SO2 là x thì nS là x và nO là 2x.
Gọi số mol SO3 là y thì nS là y và nO là 3y.
Theo đề bài ta có hệ phương trình:
(x+y)x32=2,4
và (2x+3y)x16=2,8
Giải hệ phương trình ta được x=0,05 và y=0,025
Vậy nSO2/nSO3= x/y =0,05/0,025 = 2/1
Câu 2. Ta có
dX2/C2H2 = 2,731 → MX2/MC2H2 = 2,731 → MX2=71
Nguyên tử khối của X là 71/2=35,5 đvC: clo (Cl)
Câu 3.
• S là đơn chất, vì chất này được tạo nên từ 1 nguyên tố hóa học là lưu huỳnh.
• O2 là đơn chất, vì chất này được tạo nên từ 1 nguyên tố hóa học là oxi.
• SO2 là hợp chất, vì chất này được tạo nên từ 2 nguyên tố hóa học là lưu huỳnh và oxi.
b) Theo phương trình hóa học : nO2=nS=2,5 mol
Thể tích khí oxi đktc cần dùng là: 2,5 x 22,4 = 56 (lít)
c) Khí SO2 nặng hơn không khí
Giải thích : dSO2/KK= MSO2/MKK=64/29>1
Câu 4.
a) 0,25 mol khí SO2 có khối lượng là:
mSO2=n x M =0,25 x 64 = 16 (gam)
0,25 mol khí SO2 có thể tích là:
VSO2 = n x 22,4 = 0,25 x 22,4 = 5,6 (lít)
b) Ta có : nCl2 = 10.65 / 71= 0,15(mol)
Thể tích khí Clo là : VCl2 = 0,15 x 22,4 = 3,36(lít)
Số phần tử Cl2 = 0,15 x 6.10^23 = 9.10^22 (phân tử)
Câu 5.